Анализ кщс расшифровка
Кислотно-щелочное состояние и интерпретация газового состава крови
Нарушения кислотно-щелочного состояния (КЩС) являются в большинстве случаев следствием серьезного патологического нарушения и редко имеют самостоятельное значение. Исследование газового состава артериальной крови (ГАК) — незаменимый метод диагностики у пациентов с подозрением на респираторную патологию или метаболические нарушения. Повторный анализ газового состава артериальной крови (ГАК) позволяет отслеживать течение основного заболевания и контролировать эффект проводимой терапии. Результаты исследования газового состава артериальной крови (ГАК) должны рассматриваться параллельно с оценкой клинического состояния пациента. Метод имеет ограничения, поскольку позволяет исследовать только жидкость внеклеточного компартмента и не дает информации о pH и газовом составе внутриклеточной жидкости.
Многие клиницисты сталкиваются с трудностями при интерпретации газового состава крови. В этом обзоре даются базовые сведения о газовом и кислотно-основном гомеостазе и принципы пошагового подхода к интерпретации их нарушений. Раздел, посвященный физическим аспектам, направлен на углубленное изучение рассматриваемого вопроса; при желании его можно пропустить и перейти непосредственно к клиническому приложению.
Основы физики
Показатель pH представляет собой отрицательный десятичный логарифм концентрации ионов водорода (H + ). При показателе pH = 7,0 концентрация H+ составляет 10 -7 или 1/10 7 . При этом значении pH среда является нейтральной, поскольку концентрации OH — и H + равны.
H2O → H + + OH —
При pH = 1, концентрация H + составляет 10 -1 или 1/10, среда при этом является очень концентрированной кислотой.
Анализ кщс расшифровка
Символ рН и шкалу рН (от 0 до 14) ввел в 1908 г. Сервисен. Если рН равно 7,0 (нейтральная реакция среды), то содержание ионов Н + равно 10 7 моль/л. Кислая реакция раствора имеет рН от 0 до 7; щелочная — от 7 до 14.
Кислота рассматривается как донор ионов водорода, основание — как их акцептор, т. е. вещество, которое может связывать ионы водорода.
Постоянство кислотно-основного состояния (КОС) поддерживается как физико-химическими (буферные системы), так и физиологическими механизмами компенсации (легкие, почки, печень, другие органы).
Буферными системами называют растворы, обладающие свойствами достаточно стойко сохранять постоянство концентрации водородных ионов как при добавлении кислот или щелочей, так и при разведении.
Буферная система — это смесь слабой кислоты с солью этой кислоты, образованной сильным основанием.
Примером может служить сопряженная кислотно-основная пара карбонатной буферной системы: Н2СО3 и NaHC03.
В крови существует несколько буферных систем:
2) система гемоглобин — оксигемоглобин (оксигемоглобин имеет свойства слабой кислоты, а дезоксигемоглобин — слабого основания);
3) белковая (обусловленная способностью белков ионизироваться);
4) фосфатная система (дифосфат — монофосфат).
Самой мощной является бикарбонатная буферная система — она включает 53% всей буферной емкости крови, остальные системы составляют соответственно 35%, 7% и 5%. Особое значение гемоглобинового буфера заключается в том, что кислотность гемоглобина зависит от его оксигенации, то есть газообмен кислорода потенцирует буферный эффект системы.
Исключительно высокую буферную емкость плазмы крови можно проиллюстрировать следующим примером. Если 1 мл децинормальной соляной кислоты добавить к 1 л нейтрального физиологического раствора, который не является буфером, то его рН упадет с 7,0 до 2,0. Если такое же количество соляной кислоты добавить к 1 л плазмы, то рН снизится всего с 7,4 до 7,2.
Роль почек в поддержании постоянства кислотно-основного состояния заключается в связывании или выведении ионов водорода и возвращении в кровь ионов натрия и бикарбоната. Механизмы регуляции КОС почками тесно связаны с водно-солевым обменом. Метаболическая почечная компенсация развивается гораздо медленнее дыхательной компенсации — в течение 6-12 ч.
Постоянство кислотно-основного состояния поддерживается также деятельностью печени. Большинство органических кислот в печени окисляется, а промежуточные и конечные продукты либо не имеют кислого характера, либо представляют собой летучие кислоты (углекислота), быстро удаляющиеся легкими. Молочная кислота в печени преобразуется в гликоген (животный крахмал). Большое значение имеет способность печени удалять неорганические кислоты вместе с желчью.
Выделение кислого желудочного сока и щелочных соков (панкреатического и кишечного) также имеет значение в регуляции КОС.
Огромная роль в поддержании постоянства КОС принадлежит дыханию. Через легкие в виде углекислоты выделяется 95% образующихся в организме кислых валентностей. За сутки человек выделяет около 15 ООО ммоль углекислоты, следовательно, из крови исчезает примерно такое же количество ионов водорода (Н 2 СО 3 = C02↑ + Н 2 0). Для сравнения: почки ежедневно экскретируют 40-60 ммоль Н+ в виде нелетучих кислот.
Количество выделяемой двуокиси углерода определяется ее концентрацией в воздухе альвеол и объемом вентиляции. Недостаточная вентиляция приводит к повышению парциального давления С02 в альвеолярном воздухе (альвеолярная гиперкапния) и соответственно увеличению напряжения углекислого газа в артериальной крови (артериальная гиперкапния). При гипервентиляции происходят обратные изменения — развивается альвеолярная и артериальная гипокапния.
Таким образом, напряжение углекислого газа в крови (РаСO 2 ), с одной стороны, характеризует эффективность газообмена и деятельность аппарата внешнего дыхания, с другой — является важнейшим показателем кислотно-основного состояния, его дыхательным компонентом.
Респираторные сдвиги КОС самым непосредственным образом участвуют в регуляции дыхания. Легочный механизм компенсации является чрезвычайно быстрым (коррекция изменений рН осуществляется через 1-3 мин) и очень чувствительным.
При повышении РаСO 2 с 40 до 60 мм рт. ст. минутный объем дыхания возрастает от 7 до 65 л/мин. Но при слишком большом повышении РаСO2 или длительном существовании гиперкапнии наступает угнетение дыхательного центра с понижением его чувствительности к СO2.
При ряде патологических состояний регуляторные механизмы КОС (буферные системы крови, дыхательная и выделительная системы) не могут поддерживать рН на постоянном уровне. Развиваются нарушения КОС, и в зависимости от того, в какую сторону происходит сдвиг рН, выделяют ацидоз и алкалоз.
В зависимости от причины, вызвавшей смещение рН, выделяют дыхательные (респираторные) и метаболические (обменные) нарушения КОС: дыхательный ацидоз, дыхательный алкалоз, метаболический ацидоз, метаболический алкалоз.
Системы регуляции КОС стремятся ликвидировать возникшие изменения, при этом респираторные нарушения нивелируются механизмами метаболической компенсации, а метаболические нарушения компенсируются изменениями вентиляции легких.
6.1. Показатели кислотно-основного состояния
Кислотно-основное состояние крови оценивается комплексом показателей.
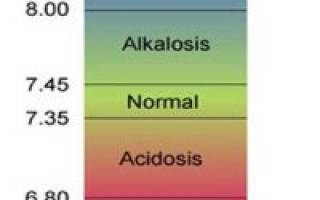
Величина рН — основной показатель КОС. У здоровых людей рН артериальной крови равен 7,40 (7,35-7,45), т.е. кровь имеет слабощелочную реакцию. Снижение величины рН означает сдвиг в кислую сторону — ацидоз (рН 7,45).
Размах колебаний рН кажется небольшим вследствие применения логарифмической шкалы. Однако разница в единицу рН означает десятикратное изменение концентрации водородных ионов. Сдвиги рН более чем на 0,4 (рН менее 7,0 и более 7,8) считаются несовместимыми с жизнью.
Колебания рН в пределах 7,35-7,45 относятся к зоне полной компенсации. Изменения рН вне пределов этой зоны трактуются следующим образом:
• субкомпенсированный ацидоз (рН 7,25-7,35);
• декомпенсированнй ацидоз (рН 7,55).
РаСO2 (РСO2) — напряжение углекислого газа в артериальной крови. В норме РаСO2 составляет 40 мм рт. ст. с колебаниями от 35 до 45 мм рт. ст. Повышение или снижение РаСO2 является признаком респираторных нарушений.
Альвеолярная гипервентиляция сопровождается снижением РаСO2 (артериальной гипокапнией) и респираторным алкалозом, альвеолярная гиповентиляция — повышением РаСO2 (артериальной гиперкапнией) и респираторным ацидозом.
Буферные основания (Buffer Base, ВВ) — общее количество всех анионов крови. Поскольку общее количество буферных оснований (в отличие от стандартных и истинных бикарбонатов) не зависит от напряжения СO2, по величине ВВ судят о метаболических нарушениях КОС. В норме содержание буферных оснований составляет 48,0 ± 2,0 ммоль/л.
Избыток или дефицит буферных оснований (Base Excess, BE) — отклонение концентрации буферных оснований от нормального уровня. В норме показатель BE равен нулю, допустимые пределы колебаний ±2,3 ммоль/л. При повышении содержания буферных оснований величина BE становится положительной (избыток оснований), при снижении — отрицательной (дефицит оснований). Величина BE является наиболее информативным показателем метаболических нарушений КОС благодаря знаку (+ или -) перед числовым выражением. Дефицит оснований, выходящий за пределы колебаний нормы, свидетельствует о наличии метаболического ацидоза, избыток — о наличии метаболического алкалоза.
Стандартные бикарбонаты (SB) — концентрация бикарбонатов в крови при стандартных условиях (рН = 7,40; РаСO2 = 40 мм рт. ст.; t = 37 °С; SO2 = 100%).
Истинные (актуальные) бикарбонаты (АВ) — концентрация бикарбонатов в крови при соответствующих конкретных условиях, имеющихся в кровеносном русле. Стандартные и истинные бикарбонаты характеризуют бикарбонатную буферную систему крови. В норме значения SB и АВ совпадают и составляют 24,0 ± 2,0 ммоль/л. Количество стандартных и истинных бикарбонатов уменьшается при метаболическом ацидозе и увеличивается при метаболическом алкалозе.
6.2. Нарушения кислотно-основного состояния
Метаболический (обменный) ацидоз развивается при накоплении в крови нелетучих кислот. Он наблюдается при гипоксии тканей, нарушениях микроциркуляции, кетоацидозе при сахарном диабете, почечной и печеночной недостаточности, шоке й других патологических состояниях. Наблюдается уменьшение величины рН, снижение содержания буферных оснований, стандартных и истинных бикарбонатов. Величина BE имеет знак (-), что свидетельствует о дефиците буферных оснований.
К метаболическому (обменному) алкалозу могут приводить тяжелые нарушения обмена электролитов, потеря кислого желудочного содержимого (например, при неукротимой рвоте), чрезмерное потребление с пищей щелочных веществ. Увеличивается значение рН (сдвиг в сторону алкалоза) — повышается концентрация ВВ, SB, АВ. Величина BE имеет знак (+) — избыток буферных оснований.
Причиной дыхательных нарушений кислотно-основного состояния является неадекватная вентиляция.
Респираторный (дыхательный) алкалоз возникает в результате произвольной и непроизвольной гипервентиляции. У здоровых людей он может наблюдаться в условиях высокогорья, при беге на длинные дистанции, при эмоциональном возбуждении. Одышка легочного или сердечного больного, когда нет условий для задержки СO2 в альвеолах, искусственная вентиляция легких могут сопровождаться респираторным алкалозом. Он протекает с повышением рН, снижением РаСO2, компенсаторным уменьшением концентрации бикарбонатов, буферных оснований, нарастанием дефицита буферных оснований.
Анализ кщс расшифровка
Анализ кислотно-щелочного состояния / равновесия / баланса (кому как больше нравится) является неотъемлемой частью быстрой оценки тяжести состояния пациента при различных патологиях. Поэтому широкое и абсолютно оправданное внедрение в клиническую практику анализа кислотно-основного равновесия и газового состава крови диктует необходимость обеспечить информационную поддержку по данной проблеме.
Первое знакомство с данной темой происходит еще на 3 курсе медицинского университета на кафедре патологической физиологии, но обычно она проходится «галопом по Европам», и на выходе при первой реальной встрече с данными, касающимися оценки кислотно-щелочного состояния (КЩС) и газового состава крови, возникает проблема. Данная информация не претендует на новаторство, однако может быть полезна как студентам, осваивающим эту тему, так и при повторении уже закончившим университет специалистам различных специальностей.
Пару вступительных слов… Что же относится к нарушениям КЩС?
Расстройства кислотно-основного равновесия (КОР) — это нарушения физико-химического гомеостаза. Кислотно-основное равновесие определяется соотношением ионов Н + и ОН – , влияющим на активность ферментов, интенсивность метаболических процессов, функции ряда органов, чувствительность рецепторов к медиаторам, проницаемость клеточных мембран. Расстройства КОР сопровождают практически все заболевания, поэтому аналогично другим видам нарушений обмена веществ относятся к типовым патологическим процессам.
Исследование газового состава артериальной крови включает определение в ней парциального давления кислорода (pO2) и углекислого газа (pCO2), рН, насыщения кислородом SaO2, концентрации HCO3.
Целями исследования газового состава крови являются:
- Оценка эффективности газообмена в легких;
- Оценка сохранности системы, регулирующей функцию дыхания;
- Определение кислотно-щелочного равновесия (КЩР) крови;
- Оценка эффективности респираторной поддержки.
Приступим непосредственно к анализу представленных вам данных. Для быстроты оценки изменений газового состава крови мы воспользуемся правилом из всеми известной игры «крестики-нолики».
Что нужно помнить для начала? Конечно же, нормы показателей. В нашем случае нас интересуют три показателя:
NB! Напомним, что:
- Ацидоз — это типовой патологический процесс, характеризующийся относительным или абсолютным понижением pH;
- Алкалоз — это типовой патологический процесс, характеризующийся относительным или абсолютным увеличением pH.
Следующим пунктом следует оценить парциальное давление углекислого газа в крови (рСО2) и концентрацию в ней бикарбонатов. Это позволит вам понять возможный тип нарушения кислотно-щелочного равновесия и характер компенсации процесса.
Ответьте для себя на вопрос: «Что является причиной сдвигов pH крови?»
NB! Напомним, что:
- рСО2 отражает респираторный компонент изменения рН, напрямую или косвенно связанный с нарушением функции легких;
- НСО3 отражает метаболический компонент изменения рН, включающий в себя нарушения работы буферных систем или функции физиологических систем, а также нарушения метаболизма в том или ином виде, приводящие к накоплению кислот.
Для наилучшего запоминания взаимозависимости изменений рН, рСО2 и концентрации HCO3 можно применять мнемоническое правило RO-ME:
Respiratory — Opposite (значение рН противоположно показателю рСО2):
- Когда рН увеличивается, рСО2уменьшается = респираторный алкалоз;
- Когда рН уменьшается, рСО2увеличивается = респираторный ацидоз.
Metabolic — Equal (значение рН изменяется синхронно с показателем изменения концентрации HCO3):
- Когда рН увеличивается, НСО3увеличивается = метаболический алкалоз;
- Когда рН уменьшается, НСО3уменьшается = метаболический ацидоз.
Постарайтесь внимательно и вдумчиво понять зависимость показателей, которые мы используем. Это поможет вам максимально быстро расшифровывать изменения газового состава крови.
Перейдем непосредственно к игре «крестики-нолики». Рисуете на листке бумаге сетку 3×3, как показано на рисунке ниже. Как мы видим, верхняя строка отражает тип нарушения КЩР.
Теперь обратимся, к примеру, к этим данным, полученным при исследовании газового состава крови пациента К., 35 лет:
pH: 7,26, pCO2: 32 мм рт. ст., HCO3: 18 ммоль/л
Начнем заполнять нашу сетку (прим. — нормальные показатели представлены в начале данного поста). Как мы видим, показатели рН и HCO3 смещаются в сторону ацидоза (Acidic), а показатель рСО2 — в сторону алкалоза (Basic).
Итак, один вертикальный ряд закрыт! Заполнены все клетки столбца «Acidic». Так как HCO3 является метаболическим компонентом, значит, данный тип изменения КЩР — метаболический ацидоз (для самопроверки не забываем про правило RO-ME).
Рассмотрим другой пример. Пациент Г., 47 лет:
pH: 7,52, pCO2: 55 мм рт. ст., HCO3: 32 ммоль/л
Как мы видим, показатели рН и НСО3 смещаются в сторону алкалоза, а показатель рСО2 — в сторону ацидоза.
Источник: https://vk.com/criticaldoc
Итак, один вертикальный ряд закрыт! Заполнены все клетки столбца «Alkalosis». Так как HCO3 является метаболическим компонентом, значит, данный тип изменения КЩР — метаболический алкалоз (для самопроверки не забываем про правило RO-ME).
Рассмотрим другой пример. Пациент О., 56 лет:
pH: 7,29, pCO2: 36 мм рт. ст., HCO3: 17 ммоль/л
В этом случае показатели рН и HCO3 смещаются в сторону ацидоза, а показатель pCO2 находится в пределах референсных значений.
Источник: https://vk.com/criticaldoc
Итак, один вертикальный ряд закрыт! Заполнен весь столбец «Acidosis». Так как HCO3 является метаболическим компонентом, то данный тип изменения КЩР — метаболический ацидоз (для самопроверки не забываем про правило RO-ME).
Теперь коснемся вопроса о компенсации изменений КЩР. Ацидоз/алкалоз может быть компенсированным, субкомпенсированным или декомпенсированным. Компенсированные формы связаны с сохранением жизнедеятельности клетки, в то время как некомпенсированные формы вызывают нарушения функции клетки. Показателем компенсации является величина рН артериальной крови.
NB! Запомните правило:
- Если рН находится в пределах нормы, а показатели pCO2 и HCO3 — нет = компенсация;
- Если рН находится за пределами нормы (в любую из сторон), а pCO2и HCO3 также вне пределов нормы = субкомпенсация (прим. — изменены все три показателя);
- Если рН находится за пределами нормы (в любую из сторон), pCO2или HCO3 также вне пределов нормы = декомпенсация (прим. — изменены только два из трех показателей).
Вернемся к нашим примерам:
Пример 1. Как мы выяснили, у нашего больного К., 35 лет, произошло изменение КЩР по типу метаболического ацидоза. Вспоминаем про правило выше. Все три показателя находятся вне пределов референсных значений, что свидетельствует о частичной компенсации. По итогу мы имеем: «Метаболический ацидоз с частичной компенсацией».
Пример 2. В этом случае у больного Г., 47 лет, произошло изменение КЩР по типу метаболического алкалоза. Все три показателя находятся вне пределов референсных значений, что свидетельствует о частичной компенсации. По итогу мы имеем: «Метаболический алкалоз с частичной респираторной компенсацией».
Пример 3. По имеющимся данным можно сделать вывод, что у нашего больного О., 56 лет, произошло изменение КЩР по типу метаболического ацидоза. Действуем по вышеуказанному правилу: только два показателя находятся за пределами своих нормальных значений (рН, HCO3), из чего следует диагноз: «Метаболический ацидоз, декомпенсированный».
И еще один пример для закрепления. Пациент И., 63 года:
pH: 7,44, pCO2: 30 мм рт. ст., HCO3: 21 ммоль/л
Казалось бы, выше мы говорили о том, что степень компенсации КЩР определяется на основании уровня рН. Что же мы видим? рН находится в пределах референсных значений, что наводит нас на мысль о том, что организм уже победил данное патологическое изменение КЩР. Но нам требуется узнать первопричину его изменения.
Хоть рН и находится в пределах нормы (рН: 7,44), но все же он является «слегка щелочным». По итогу условно примем, что показатель рН смещен больше в сторону столбца «Basic», а значит у данного больного изначально развился «респираторный алкалоз». Смещение показателя HCO3 в сторону столбца «Acidic» свидетельствует о том, что организм смог включить компенсаторный механизм и привести рН в пределы нормальных значений. По итогу в данном случае мы имеем: «Респираторный алкалоз, компенсированный».
Для закрепления вышеизложенной информации предлагаем вам посмотреть следующие видео:
Также для быстрой оценки нарушений КЩС можно использовать номограмму Siggaard-Andersen:
Источник:
Анализ нарушений кислотно-щелочного состояния
р Н а р т е р и а л ь н о й к р о в и
АЦИДОЗ (меньше 7.4) АЛКАЛОЗ (больше 7.4)
дыхательный недыхательный дыхательный недыхательный
почечная легочная почечная легочная
компенсация компенсация компенсация компенсация
Нарушения кислотно-щелочного состояния (КЩС) являются в большинстве случаев следствием серьезного патологического нарушения и редко имеют самостоятельное значение. Исследование газового состава артериальной крови (ГАК) — незаменимый метод диагностики.
♦ Обычно pH измеряют прямым методом при помощи специального стеклянного электрода, который имеет мембрану, проницаемую для H+.
♦ Концентрация ионов бикарбоната — HCO3 — измеряется бикарбонатным электродом или может быть получена расчетным путем.
♦ CO2 обычно измеряется прямым методом при помощи СО2-электрода.
Бикарбонатная система участвует в регуляции pH всех компартментов внутренней среды, обладая возможностью вмешиваться в кислотно-щелочное состояние на двух уровнях: концентрация HCO3 — регулируется почками, a CO2 – легкими: H + + HCO3 — → H2CO3 → H2O + CO2
Точное значение pH среды может быть рассчитано при помощи уравнения Гендерсона-Хассельбаха:
pH = pK + log
[основание] / [кислота] = pK + log [HCO3 — ] / [H2CO3]
pK представляет собой специфичную для данного буфера константу (например, для бикарбонатной системы при 37°С pK составляет 6,1).
Поскольку концентрация HCO3 — регулируется почками, а выведение CO2 — легкими, уравнение принимает следующий вид: pH = константа ПОЧКИ / ЛЕГКИЕ
Терминологические замечания: ацидоз / ацидемия и алкалоз / алкалемия. Суффикс «емия» («aemia») означает «определяемый в крови».
Бикарбонатная буферная система играет наиболее важную роль в поддержание постоянства кислотно-щелочного состояния и может быть оценена при анализе газового состава крови. Легкие способны регулировать выведение CO2, а почки экскрецию или задержку HCO3 — . Это взаимодействие позволяет с высокой точностью поддерживать и регулировать соотношение кислот и оснований в организме.
Дыхательная система способна осуществлять быструю компенсацию нарушений кислотно-щелочного состояния (КЩС) (в течение нескольких минут). Метаболическая компенсация (почки, система бикарбоната) запускается в течение часов или нескольких дней. Взаимодействие этих компенсаторных систем позволяет точно регулировать кислотно-щелочного состояние (КЩС). Их цель состоит в поддержании внеклеточного значения pH на уровне 7,4, который является оптимальным для протекания большинства метаболических процессов, например, химических реакций, катализируемых ферментами, и переноса веществ через клеточные мембраны.
Патологические процессы, такие, как тканевая гипоксия, почечная недостаточность, гиповентиляция ведут к нарушению кислотно-щелочного баланса. При нарушении со стороны одной из регуляторных систем другая будет пытаться компенсировать изменения кислотно-щелочного состояния (КЩС) и привести pH к оптимальному значению. Нарушения кислотно-щелочного состояния (КЩС) и некоторые их причины представлены в таблице «Нарушения кислотно-щелочного состояния«.
Компенсаторные механизмы пытаются вернуть pH к нормальному значению, несмотря на сохранение отклонений [HCO3 — ] и PCO2 до коррекции первичного нарушения. Компенсация нарушений кислотно-щелочного состояния (КЩС) не должна носить характер избыточной. Например, при метаболическом ацидозе наблюдается падение значения pH
Вот несколько подсказок, которые помогут Вам дифференцировать первичное нарушение и компенсаторный эффект.
Первичное нарушение (метаболического или респираторного характера) по типу параллельно отклонению pH: при снижении pH имеет место ацидотическое нарушение, при повышении pH развивается алкалоз. Компенсаторный эффект (респираторный или метаболический) имеет противоположное направление. Механизмы компенсации будут отклонять pH в сторону нормального значения, при этом полная компенсация достигается редко (восстановление нормального исходного значения), а избыточная компенсация — никогда.
К примеру, если Вы обнаружили сочетание метаболического ацидоза и респираторного алкалоза, значение pH подскажет, какое из нарушений носит первичный, а какое — компенсаторный характер. Если значение pH снижено, первичным дефектом является метаболический ацидоз с респираторной компенсацией. При повышении pH в роли первичного нарушения выступает респираторный алкалоз с метаболической компенсацией.
Немаловажно учитывать при оценке кислотно-основного состояния организма РаС02, т.е. напряжение углекислого газа в артериальной крови. В норме данный показатель составляет в среднем 40 мм рт. ст. (от 35 до 45), а более значительные отклонения от нормы являются признаком дыхательных нарушений.
Метаболический алкалоз или ацидоз определяется в том числе по избытку или недостаточности буферных оснований (Buffer Base, ВВ) в крови. У здорового человека В В = 0, а допустимые пределы колебаний составляют ±2,3 ммоль/л.
Такой показатель как «стандартные бикарбонаты» (SB) отражает концентрацию бикарбонатов в крови при стандартных условиях (рН = 7,40; РаС02 = 40 мм рт. ст.; t = 37 °С; S02 = 100%). «Истинные, или актуальные бикарбонаты» (АВ) отражают состояние бикарбонатного буфера в условиях конкретного организма, в норме совпадают со «стандартными» и составляют 24,0 ± 2,0 ммоль/л.
Показатели SB и АВ снижаются при нарушение обмена веществ со сдвигом реакции крови в кислую сторону и уменьшаются при сдвиге реакции крови в щелочную сторону.
Если лабораторные данные свидетельствуют о наличии метаболического ацидоза, это может быть признаком кетоацидоза, сахарного диабета, кислородного голодания (гипоксии) тканей, шокового состояния, а также ряда других патологических состояний.
Причиной метаболического алкалоза может стать неукротимая рвота (с большой потерей кислоты с желудочным соком) или чрезмерное употребление в пищу продуктов, вызывающих ощелачивание организма (растительных, молочных).
Дыхательный алкалоз может возникнуть у физически здорового человека в условиях высокогорья или при чрезмерной физической или психической нагрузке. Также он отмечается при одышке у пациентов с заболеваниями сердца и (или) легких, если углекислый газ не скапливается в легочных альвеолах.
Дыхательный ацидоз развивается при недостаточном поступлении воздуха в легкие, что может говорить об угнетении деятельности дыхательного центра в головном мозге, выраженной дыхательной недостаточности при тяжелой патологии легких.
7. Показатели осмотического и онкотического давления крови. Значение. Учебник
8. Определение осмотической резистентности эритроцитов Работа 3.5 – стр. 82
Определение осмотической резистентности эритроцитов (осмотической стойкости): используют набор гипотонических растворов NaCl (концентрация соли ниже 0.9%), помещают в них эритроциты исследуемой крови и отмечают концентрацию раствора, в котором (а) начинается гемолиз отдельных эритроцитов (в норме 0.48% NaCl и (б) происходит полный гемолиз всех эритроцитов (в норме 0.33% NaCl). Например, осмотическая стойкость эритроцитов уменьшается при сфероцитозе и увеличивается при талассемии.
9. Исследование буферных свойств сыворотки крови (опыт Фриденталя). Учебник
Показатель рН – 7.35 – 7.4(отрицательный логарифм концентрации водородных ионов) – влияет на ход всех биохимических реакций в организме. Сдвиг рН в кислую сторону называется ацидозом, сдвиг в щелочную сторону – алкалозом. Регуляция рН:(1) В крови имеются буферные системы, которые могут связывать водородные и гидроксильные ионы и, таким образом, уменьшать колебания рН (доли секунды); (2) дыхательная система – удаление СО2 легкими (несколько минут); (3) выделительная функция почек – выведение кислых и щелочных продуктов обмена; самый медленный механизм (часы, дни), но самый мощный. Буферные системы крови: (1) бикарбонатный буфер (угольная кислота и бикарбонат натрия) – буферная система крови; (2) фосфатный буфер (гидрофосфат и дигидрофосфат натрия) – буферная система крови, почечных канальцев, а также внутриклеточная буферная система многих тканей; (3) гемоглобиновый буфер (восстановленный гемоглобин ННв и калиевая соль оксигенированного гемоглобина КНвО2) – буферная система эритроцитов, самая мощная (75% общей буферной емкости); (4) белковый буфер (амфолитные свойства белков) – буферная система крови, а также внутриклеточная буферная система.
Дата добавления: 2015-07-22 ; просмотров: 5386 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Физиология и нарушения кислотно-основного состояния (методические материалы к практическим и семинарским занятиям)
Информация
Справочное пособие содержит информацию о физиологии кислотно- основного состояния (КОС). Представлена информация о методах лабораторной диагностики нарушений КОС. Перечислены варианты нарушений и методы коррекции. Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
Физиология кислотно-основного состояния
В норме сильных кислот образуется 50 – 100 ммоль/сутки. При избыточном образовании они вызывают тяжелые нарушения. Это происходит при анаэробном окислении глюкозы.
В норме окисление глюкозы происходит аэробно: С6Н12О2 + 6О2 = 6Н2О + 6СО2 + 38 АТФ
Рис. 1. Доставка 02 к тканям и первые стадии элиминации CO2
Рис. 2. В легких бикарбонат снова превращается в С02 и выводится
Транспорт кислорода из легких к тканям и из тканей к легким обусловлен изменениями, которые воздействуют на сродство кислорода к гемоглобину. На уровне тканей из-за снижения рН это сродство уменьшается (эффект Бора) и вследствие этого улучшается отдача кислорода. В крови легочных капилляров сродство гемоглобина к кислороду увеличивается из-за снижения рС02 и возрастания рН по сравнению с аналогичными показателями венозной крови, что приводит к повышению насыщения артериальной крови кислородом.
Первичные изменения КЩС и компенсаторные реакции