Инфаркт миокарда кфк это
Инфаркт миокарда кфк это
Общий анализ крови. При инфаркте миокарда отмечается лейкоцитоз, который наиболее выражен через 2—4 дня от начала развития коронарной катастрофы. Количество лейкоцитов в 1 мм3 увеличивается обычно до 12 000—15 000, иногда до 20 000, к нормальному уровню возвращается через неделю от начала развития инфаркта миокарда (В. J. Gersh, I. P. Clements, 1996).
Отмечается сдвиг формулы влево с увеличением количества полинуклеаров. Как отмечают авторы, речь идёт только о тех случаях, когда отсутствует другой патологический процесс, вызывающий лимфоцитопению.
Определение активности креатинфосфокиназы (КФК) и её МВ-фракции в плазме крови было и остаётся надёжным методом лабораторной диагностики поражения сердечной мышцы у больных инфарктом миокарда. Некроз порядка 0,1 г миокарда можно определить, измеряя МВ-фракцию КФК в динамике (при поступлении, а затем с интервалом в 4—8 ч в течение 24 ч). Известны три изофермента креатинфосфокиназы: изофермент ММ содержится преимущественно в скелетных мышцах, ВВ («би-би») — в мозге и почках, MB («эм-би») — в сердце.
Подъём в крови MB-КФК наблюдается при инфаркте раньше, чем общей КФК. Сейчас в клинике также активно изучается роль под фракций MB-КФК, в частности соотношения между МВ2 и МВР в ранней диагностике инфаркта миокарда (самые первые часы развития коронарной катастрофы). Так как концентрация кардиоспецифических тропонинов может оставаться повышенной спустя несколько суток (до 2 недель) от развития коронарной катастрофы, их определение не может полностью «вытеснить» анализ активности в крови КФК и её МВ-фракции, которые помогают определить «свежесть» инфаркта.
При успешной реперфузии активность КФК нарастает быстрее с достижением раннего пика (до 24 ч от начала развития инфаркта миокарда), чем при сохраняющейся закупорке венечной артерии. Следует заметить, что динамика общей активности КФК в плазме крови не столько помогает в ранней диагностике инфаркта миокарда, сколько позволяет косвенно судить о величине поражения мышцы сердца.
Напомним, что содержащийся в миокарде МВ-изофермент КФК присутствует в небольшом количестве также и в скелетных мышцах, тонком кишечнике, лёгких, диафрагме, матке и простате. Поэтому содержание в крови МВ-фракции КФК может повышаться при целом ряде состояний в отсутствие инфаркта миокарда. Например, при бронхиальной астме, гипервентиляции лёгких, тромбоэмболии гочной артерии, остром либо хроническом поражении мышечного аппарата (вклю внутримышечные инъекции, физические перегрузки, тремор при алкогольной стиненции, судороги, рабдомиолиз на фоне приёма таких гиполипидемических препаратов, как ингибиторы ГМГ-КоА-редуктазы), во время и после родов, при почечной недостаточности, гипотиреозе и других состояниях. Это может приводить к ложноположительной диагностике коронарной катастрофы.
Не следует забывать и о возможном кардиогенном подъёме МВ-фракции КФК, не связанном с инфарктом миокарда. Например, при дефибрилляции, закрытой травме сердца (удар о руль при автокатастрофе), операции на сердце, миокардите, перикардите. Поэтому лабораторные данные надо всегда рассматривать с учётом клиники.
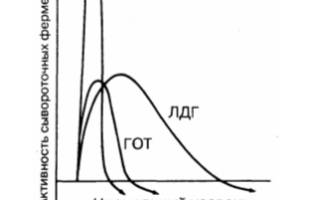
Динамика сывороточных ферментов после типичного инфаркта миокарда.
КФК — креатинфосфокиназа; ЛДГ — лактатдегидрогеназа; ГОТ — глутаматрксалоацетаттрансаминаза.
61.Биохимическая диагностика инфаркта миокарда. Креатинкиназа. Лактатдегидрогеназа. Другие биохимические показатели повреждения миокарда.
При инфаркте миокарда (ИМ) в результате некроза клеток сердечной мышцы в кровеносное русло попадают содержащиеся в них ферменты и белки. По их наличию, времени появления и концентрации в плазме крови можно оценить ущерб, нанесенный сердечной мышце. Эти сведения дополняют данные ЭКГ и помогают в ранней диагностике ИМ, что позволяет своевременно избрать правильную тактику лечения.
Идеальный биохимический маркер должен обладать наивысшей специфичностью и чувствительностью в отношении некроза миокарда, в течение короткого времени после начала симптомов ИМ достигать в крови диагностически значимого уровня, этот уровень должен сохраняться в течение многих дней. В настоящее время маркера, полностью отвечающего всем этим требованиям, не существует, поэтому для диагностики ИМ рекомендуется параллельно использовать два маркера — «ранний» и «поздний». Содержание «раннего» маркера при ИМ диагностически значимо повышается в крови в первые часы заболевания, «поздний» —достигает диагностически значимого уровня только через 6—9 ч, но обладает высокой специфичностью в отношении некроза миокарда.
Ранние маркеры некроза миокарда:
МВ-КФК (сердечная форма креатинфосфокиназы — КФК)
Сердечная форма белка, связывающего жирные кислоты (сБСЖК)
Поздние маркеры некроза миокарда:
Сердечные тропонины I и Т
Среди множества биохимических маркеров, которые могут менять свою концентрацию в плазме крови при ИМ, наиболее кардиоспецифическими являются тропонины, МВ-фракция креатенинфосфокиназы (КФК-МВ) и миоглобулин, которые и представляют наибольшую диагностическую ценность.
Тропонин — является ферментом «быстрого реагирования», поскольку попадает в периферический кровоток из зоны некроза уже в первые часы повреждения миокарда. Тропонины Т и I присутствуют только в клетках миокарда, поэтому повышение их концентрации в крови является достоверным признаком ИМ и показателем его распространенности. Отрицательный тропониновый тест вначале сердечного приступа и через 12 часов позволяет исключить у больного ИМ и диагностировать нестабильную стенокардию. Даже незначительное повышение уровня тропонинов в периферической крови через 6-12 часов после болевого приступа расценивается как признак ишемии миокарда ведущей к некрозу и позволяет выявить ИМ без явных клинических симптомов и ЭКГ-признаков заболевания.
МВ-фракция креатенинфосфокиназы (МВ-КФК) содержится преимущественно в клетках миокарда, но в небольшом количестве присутствует и в скелетных мышцах, поэтому активность этого фермента в крови может повышаться при повреждении не только сердечной мышцы, но и других мышечных групп. Судить о повреждении миокарда на фоне сердечного приступа позволяет нарастание активности МВ-КФК в динамике. Для диагностики ИМ в первые сутки от начала сердечного приступа ее определяют 2-3 раза каждые 8 часов. Три отрицательных результата позволяют исключить ИМ, а нарастание концентрации этого фермента в крови с высокой долей вероятности свидетельствует об ИМ. Уровень активности MB — КФК позволяет определить величину инфаркта миокарда и тяжесть заболевания.
Миоглобин — очень ранний и чувствительный, но менее специфичный маркер ИМ, поскольку содержание этого мышечного белка в крови может увеличиваться и по другим причинам. Миоглобин при сердечном приступе появляется в крови еще до формирования очага некроза, на стадии выраженного ишемического повреждения сердечной мышцы. Повышение уровня миоглобина в 10 раз и больше указывает на некроз мышечных клеток.
Лактатдегидрогеназа (ЛДГ) — фермент, принимающий участие в реакциях гликолиза, катализируя превращение лактата в пируват, при этом образуется NADH. ЛДГ имеет пять изо-энзимов. В сердечной мышце содержится преимущественно изоэнзим ЛДГ-1. При ИМ концентрация ЛДГ начинает превышать нормальный уровень через 14—48 ч после начала симптомов, достигает максимального значения на 3—6-е сутки заболевания и возвращается к норме на 7—14-е сутки болезни. ЛДГ-1 была обнаружена также в эритроцитах, почках, мозге, желудке, повышение концентрации этого белка в крови больных далеко не всегда связано с некрозом миокарда. Отношение ЛДГ-1/ЛДГ-2, превышающее 0,76, обладает 90% специфичностью при выявлении некроза миокарда. Это соотношение может увеличиваться и в случае отсутствия ИМ, если у больного имеются массивный гемолиз, мегалобластическая анемия, распространенное повреждение скелетных мышц, тяжелое заболевание печени. Из-за позднего повышения концентрации ЛДГ в сыворотке крови этот маркер не применяется для ранней диагностики ИМ и суждения об успехе тромболитической терапии, однако ЛДГ длительно использовалась для диагностики ИМ в поздние сроки заболевания.
Аспартатаминотрансфераза (АсАТ) – фермент, который катализирует преобращение оксалоацетата в аспартат, перенося NH3 на первую молекулу. Вторым продуктом реакции является α-кетоглутарат. Реакция играет важную роль в высвобождении NH3 из аминокислот, который затем перерабатывается в цикле мочевины, так как аспартат, полученный в процессе реакции, нужен для образования аргининосукцината. У больных ИМ уровень АсАТ превышает норму через 8—12 ч после начала боли, достигает максимального значения к 24—З6-му часу и возвращается к норме за 3—4 дня. Большое количество этого фермента содержится в тканях печени, что сильно снижает его специфичность в отношении некроза миокарда. АсАТ неудобна как для ранней, так и для поздней диагностики ИМ, она используется только в сочетании с более чувствительными и специфичными маркерами. Низкая специфичность в отношении некроза миокарда послужила причиной того, что использование этого маркера, как и ЛДГ, для диагностики ИМ в настоящее время также признано нецелесообразным..
Повышение АСТ, превышающее повышение АЛТ, характерно для повреждения сердечной мышцы; если же показатель АЛТ выше, чем АСТ, то это, как правило, свидетельствует о разрушении клеток печени.
Неспецифическая реакция на повреждение миокарда включает нейтрофильный лейкоцитоз (появляется через несколько часов после окклюзии и длится 3-7 сут, число лейкоцитов достигает 12000-15000 в мкл). СОЭ повышается медленнее, достигает пика в 1-ю неделю и часто остается повышенной в течение 1-2 нед.
сБСЖК по последовательности аминокислот идентичен БСЖК, содержащемуся в поперечнополосатой мышечной ткани скелетных мышц, однако представлен в скелетной мускулатуре в минимальном количестве. Максимальное количество сБСЖК находится в ткани миокарда — 0,5 мг/г. Единственная мышца, в которой имеется относительно большое количество сБСЖК, — это диафрагма (примерно 25% от содержания в ткани миокарда). Некоторое количество сБСЖК содержится в тканях аорты, и можно предположить, что содержание его повышается, в крови при расслаивающей аневризме аорты. Так как сБСЖК в основном свободно расположен в цитоплазме клеток, в случае повреждения клеточной мембраны кардиомиоцита он быстро попадает в кровоток. В крови здоровых людей циркулирует небольшое количество сБСЖК.
Показатель КФК крови: что это, причины изменений
КФК крови – это фермент, участвующий в образовании энергии для сокращения мышц. В норме его уровень в крови невысокий (до 200 Ед/л у взрослых), но при повреждении мышц он увеличивается в 3-30 раз. Этот признак дает возможность выявить признаки инфаркта миокарда по анализам крови уже в первые часы его развития, особенно информативно определение МВ-КФК.
У детей креатинкиназа повышена при наследственной мышечной слабости (миопатии), миокардите. В любом возрасте высокие показатели бывают при травме, физических перегрузках, опухоли, гипотиреозе. Чтобы не получить ложный результат, важно на 3 дня прекратить тренировки, отказаться от алкоголя.
📌 Читайте в этой статье
КФК крови: что это
КФК крови – это уровень фермента креатинфосфокиназы, отвечающего за получение энергии. Анализ показывает разрушение мышечной ткани при болезнях скелетных мышц (миопатия, миастения), травмах, тренировках большой интенсивности.
Активность возрастает при инфаркте миокарда, что используется в лабораторных тестах, информативно исследование МВ-фракции креатинкиназы (изофермент). У ребенка определение КФК нужно при подозрении на миокардит, наследственные болезни мышц, опухоли, поражение щитовидной железы. На анализ направляет кардиолог, эндокринолог, онколог, невропатолог.
А здесь подробнее о ферментах при инфаркте.
КФК крови: что показывает у женщин и мужчин
Анализ крови на КФК показывает интенсивность разрушения мышц у мужчин и женщин. Креатинфосфокиназа, креатинкиназа (КФК) – это названия фермента. Он обеспечивает сокращение мышечных волокон и получение энергии тканями (забирает фосфат у АТФ и присоединяет его к креатину). Основное количество КФК находится в мышцах скелета и сердечной, меньше содержит головной мозг.
В норме в крови фермента мало, но уровень резко возрастает при повреждении мышечных волокон (травма, интенсивные тренировки, инфаркт). В спинномозговой жидкости, а потом и в крови возможен рост при опухолевом процессе в головном мозге.

Активность КФК зависит от пола, она выше у мужчин, возраста – дети из-за стремительного роста мышц в норме имеют большие показатели, а также физических нагрузок – у спортсменов при перетренированности отмечается возрастание активности фермента.
Изоферменты креатинкиназы
Фермент КФК состоит из 2 единиц – М и В, при их вариантах соединений образуются изоферменты креатинкиназы:
Определение активности креатинкиназы в крови у ребенка
Активность креатинкиназы – это ее уровень в крови, определение у ребенка используется в процессе диагностики:
- болезней сердца – миокардит (воспаление сердечной мышцы);
- патологий мышц – врожденные синдромы с мышечной слабостью (миопатия), они чаще всего проявляются в детском и юношеском возрасте;
- опухолевых процессов;
- заболеваний щитовидной железы, которые сопровождаются быстрой утомляемостью, ослаблением мышц (гипотиреоз, тиреотоксикоз).
Определение креатинкиназы при миокардите
Как меняется показатель при инфаркте
Динамика изменений креатинфосфокиназы, а особенно ее МВ-фракции (МВ-КФК) помогает выявить инфаркт миокарда на ранней стадии, оценить степень разрушения и риск осложнений, рецидива, а также следить за состоянием пациента в процессе восстановления.
Установлены закономерности нарастания и снижения активности фермента по мере развития инфаркта:
- рост с первых 2 часов от начала приступа загрудинной боли;
- достижение максимального уровня к 18-30 часу;
- нормализация к 3 дню при неглубоком и локальном поражении и к 5-6 при обширном;
- степень повышения – от 3 до 30 раз.
Показатель креатинфосфокиназы при инфаркте миокарда
Важно, что при стенокардии рост КФК незначительный, или фермент в норме. Это помогает правильной постановке диагноза и назначению терапии.
Кто направляет на анализ
На анализ может направить:
Нет смысла проводить исследование КФК при наличии травмы, так как уровень будет высоким, что не дает возможности выявить заболевание. Например, если при развитии инфаркта миокарда пациент упал из-за потери сознания, то ему показан анализ на тропонин, а КФК и МВ-КФК не назначают.
Биохимия крови КФК: норма в показателях
В результатах анализа (биохимия крови) норма в показателях КФК общего у взрослых мужчин и женщин отличается, у детей по возрасту также есть разница значений, верхний предел (максимальный уровень) приведен в таблице в ЕД/л.
КФК МВ-фракция в норме не должна быть выше 25 Ед/л вне зависимости от возраста и половой принадлежности.
Креатинкиназа в крови повышена: причины
Причины повышения креатинкиназы в крови у взрослого чаще всего связаны с болезнями сердца (инфаркт, миокардиодистрофия), а у ребенка это обычно означает миокардит (воспаление сердечной мышцы) или миопатию. Вне зависимости от возраста рост показателей вызывают травма, физическое перенапряжение, прием медикаментов.
Для лечения необходимо устранение причины повышения, диета с преобладанием растительной пищи и нежирного белка, важен отказ от алкоголя. У детей при миопатии применяют витамины и стимуляторы мышечных сокращений.
Изменения у взрослых
У взрослых повышение креатинкиназы означает развитие одного из заболеваний:
- миокарда – инфаркт, дистрофия (слабость сокращений), нестабильная стенокардия;
- скелетных мышц – дерматомиозит, миозит, миопатия, дистрофия, травма;
- глубокие ожоги;
- опухолевый процесс (чаще мочевой пузырь, кишечник, матка, простата);
- повреждение головного, спинного мозга;
- судорожный синдром;
- низкая функция щитовидной железы – гипотиреоз.
Нестабильная стенокардия — одна из причина повышенной креатинкиназы
К временным причинам повышения относятся:
- операции;
- прием алкоголя, наркотиков;
- лечение препаратами, снижающими уровень холестерина в крови, обезболивающие, некоторые антибиотики (например, Цифран), противоопухолевые;
- внутримышечные, внутривенные инъекции (курс);
- интенсивная физическая нагрузка, особенно при недостатке отдыха, превышающая возможности организма.
Методы коррекции
При чрезмерных физических нагрузках необходим перерыв для восстановления на 7-10 дней для нормализации КФК. Уровень фермента снизится после лечения болезни, вызвавшей отклонения. Рекомендуется в питании уменьшать потребление жирных мясных продуктов и повысить долю растительной пищи, рыбы, пить не менее 1,5 литров воды. Важно полностью исключить прием алкоголя.
Смотрите на видео о нормализации креатинкиназы:
Креатинфосфокиназа в крови повышена: причины, как лечить у детей
Если креатинфосфокиназа повышена в крови у детей, то причины могут быть связаны с наследственной миопатией, ее лечение симптоматическое:
- витамины группы В, Е;
- микроэлементы – калий и кальций в солевых растворах (внутривенно или при электрофорезе);
- прием АТФ в таблетках или инъекциях;
- аминокислоты – глютаминовая, Церебролизин;
- стимуляторы сокращений – Галантамин, Нивалин;
- массаж и лечебная физкультура.
Причины снижения
Для КФК даже полное отсутствие в крови – это вариант нормы, но если неоднократно обнаруживают показатели до 10 единиц, то это может быть признаком:
- беременности;
- повышенной гормональной активности щитовидной железы – гипертиреоз;
- алкогольного гепатита;
- ревматизма, ревматоидного артрита;
- системной склеродермии;
- тяжелой атрофии (уменьшения объема) мышц;
- длительного пребывания на постельном режиме;
- продолжительного употребления Аспирина и витамина С.
Важно учитывать, что эти состояния снизят информативность диагностики, то есть не позволят выявить повышение КФК (например, при инфаркте миокарда).
Как правильно сдавать анализ крови на мышечные ферменты
Для того чтобы получить достоверный результат анализа крови на мышечные ферменты (КФК и МВ-КФК), необходимо:
- за 3 дня отказаться от спортивных тренировок и физической работы;
- за сутки не употреблять алкоголь;
- сдавать кровь натощак (последний прием пищи до анализа должен быть в интервале от 8 до 14 часов);
- не ограничивать питьевую воду;
- согласовать с врачом прием препаратов, которые могут влиять на итоги диагностики (за 3-5 дней);
- за полчаса до взятия крови не курить, находиться в состоянии физического и психологического покоя.
А здесь подробнее о показателе ГГТ в анализе крови.
Фермент КФК в крови отражает процесс разрушения мышечной ткани. Его активность повышена при инфаркте миокарда, миокардите, миокардиодистрофии, миопатии. Повлиять на рост показателей может физическая активность, гипотиреоз. Анализ назначается для ранней диагностики инфаркта (вместе с МВ-КФК), а также при синдроме мышечной слабости, подозрении на опухолевый процесс и болезни щитовидной железы.
Снижение активности фермента может указать на слабую двигательную активность, болезни соединительной ткани. Ложные показатели бывают на фоне приема медикаментов, алкоголя. Для нормализации показателей необходимо устранение фонового заболевания, а при физических перегрузках важен отдых для восстановления мышц.
Полезное видео
Смотрите на видео об анализе крови на КФК:

Абдоминальная форма инфаркта миокарда схожа с обычными проблемами ЖКТ. Важно понять симптомы и способы диагностики, чтобы не упустить минуты на спасение.

Если есть подозрения на патологию миокарда, придется сдать анализы на ИБС. Они включают как общий анализ крови, биохимический, так и вспомогательные анализы при стенокардии.

Довольно важен ГГТ в анализе крови. В основном причины изменения у взрослых заключаются в наличии проблем с печенью, у женщин и мужчин это также может свидетельствовать о наличии патологии. Какова норма в биохимическом анализе? Причин повышения в сыворотке крови, а также как понизить показатель?

Проводится анализ на ревмопробы при подозрении на воспаления, после перенесенных заболеваний, которые могут отразиться на суставах, спровоцировать поражение органов. Какие входят анализы на ревмопробы? Как сдавать их правильно? О чем расскажет расшифровка показателей?

Не на 100%, но достаточно результативными будут ферменты при инфаркте. Кардиоспецифические ферменты помогают установить объем некроза миокарда, отличить от стенокардии и прочих проблем.

Определяют протеин в крови при подозрениях на многие патологии, в том числе онкологию. Анализ помогает определить норму, повышенные показатели реактивного с и протеина s. Стоит разобраться и со значениями: кровь на эозинофильный катионный протеин, тотал. Сгущает или нет кровь?

Лабораторная диагностика инфаркта миокарда включает общие анализы крови и мочи. Своевременность проведения, правильная расшифровка поможет назначить лечение.

Причины возникновения мелкоочагового инфаркта миокарда схожи со всеми остальными видами. Довольно непросто его диагностировать, острый на ЭКГ имеет атипичную картину. Последствия при своевременном лечении и реабилитации намного легче, чем при обычном инфаркте.

Довольно сложно поддается диагностике, поскольку довольно часто имеет аномальное течение субэндокардиальный инфаркт миокарда. Обычно его выявляют при помощи ЭКГ и лабораторных методов обследования. Острый инфаркт грозит смертью пациенту.
Инфаркт миокарда
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
Общие сведения
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза. После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда.
Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности. Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. е. формирование постинфарктного рубца.
В клиническом течении инфаркта миокарда выделяют пять периодов:
- 1 период – предынфарктный (продромальный): учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель;
- 2 период – острейший: от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов;
- 3 период – острый: от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток;
- 4 период – подострый: начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4-8 недель;
- 5 период – постинфарктный: созревание рубца, адаптация миокарда к новым условиям функционирования.
Причины инфаркта миокарда
Инфаркт миокарда является острой формой ИБС. В 97—98% случаев основой для развития инфаркта миокарда служит атеросклеротическое поражение венечных артерий, вызывающее сужение их просвета. Нередко к атеросклерозу артерий присоединяется острый тромбоз пораженного участка сосуда, вызывающий полное или частичное прекращение кровоснабжения соответствующей области сердечной мышцы. Тромбообразованию способствует повышенная вязкость крови, наблюдаемая у пациентов с ИБС. В ряде случаев инфаркт миокарда возникает на фоне спазма ветвей венечных артерий.
Развитию инфаркта миокарда способствуют сахарный диабет, гипертоничесая болезнь, ожирение, нервно-психическое напряжение, увлечение алкоголем, курение. Резкое физическое или эмоциональное напряжение на фоне ИБС и стенокардии может спровоцировать развитие инфаркта миокарда. Чаще развивается инфаркт миокарда левого желудочка.
Классификация инфаркта миокарда
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда:
На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов). В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией.
В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда:
- трансмуральный — с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый)
- интрамуральный – с некрозом в толще миокарда
- субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду
- субэпикардиальный — с некрозом миокарда в зоне прилегания к эпикарду
По изменениям, фиксируемым на ЭКГ, различают:
- «Q-инфаркт» — с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда)
- «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда)
По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на:
- правожелудочковый
- левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки
По кратности возникновения различают инфаркт миокарда:
- первичный
- рецидивирующий (развивается в срок 8 недель после первичного)
- повторный (развивается спустя 8 недель после предыдущего)
По развитию осложнений инфаркт миокарда подразделяется на:
По наличию и локализации болевого синдрома выделяют формы инфаркта миокарда:
- типичную – с локализацией боли за грудиной или в прекардиальной области
- атипичные — с атипичными болевыми проявлениями:
- периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная)
- безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная
- малосимптомную (стертую)
- комбинированную
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
- стадию ишемии (острейший период)
- стадию некроза (острый период)
- стадию организации (подострый период)
- стадию рубцевания (постинфарктный период)
Симптомы инфаркта миокарда
Предынфарктный (продромальный) период
Около 43% пациентов отмечают внезапное развитие инфаркта миокарда, у большей же части больных наблюдается различный по продолжительности период нестабильной прогрессирующей стенокардии.
Острейший период
Типичные случаи инфаркта миокарда характеризуются чрезвычайно интенсивным болевым синдромом с локализацией болей в грудной клетке и иррадиацией в левое плечо, шею, зубы, ухо, ключицу, нижнюю челюсть, межлопаточную зону. Характер болей может быть сжимающим, распирающим, жгучим, давящим, острым («кинжальным»). Чем больше зона поражения миокарда, тем более выражена боль.
Болевой приступ протекает волнообразно (то усиливаясь, то ослабевая), продолжается от 30 минут до нескольких часов, а иногда и суток, не купируется повторным приемом нитроглицерина. Боль сопряжена с резкой слабостью, возбуждением, чувством страха, одышкой.
Возможно атипичное течение острейшего периода инфаркта миокарда.
У пациентов отмечается резкая бледность кожных покровов, липкий холодный пот, акроцианоз, беспокойство. Артериальное давление в период приступа повышено, затем умеренно или резко снижается по сравнению с исходным (систолическое
Лабораторная диагностика инфаркта миокарда
Острый инфаркт миокарда (ОИМ) — некроз отдельных участков сердечной мышцы на почве острой ишемии, возникшей в результате несоответствия коронарного кровообращения потребности миокарда в кислороде.
Диагностика ОИМ базируется на обнаружении характерных клинических, лабораторных и ЭКГ-признаков. В основе лабораторной диагностики ОИМ лежит исследование активности ряда ферментов в крови и показателей общего анализа крови, лейкоформулы, электролитов, коагулограммы, КЩР.
При поступлении в стационар у больного с клиническими признаками инфаркта миокарда желательно определить следующий набор тестов: АсАТ, КФКобщ и МВ-КФК, ЛДГобщ и ЛДГ1-2, тропонины Т и/или I, уровень миоглобина. Для диагностики OИM важен исходный уровень этих маркеров и их изменения в динамике. К дополнительным маркерам, позволяющим диагностировать повреждение миокарда и прогнозировать течение заболевания, относят: уровень малонового диальдегида, ГТТФ, ВВ-изофермента гликогенфосфорилазы, Д-димера. Тесты этой группы определяются не у всех больных.
Определение активности АсАТ
В типичных случаях ОИМ активность АсАТ начинает увеличиваться через 6-8 ч после начата приступа боли, достигает максимума через 18-36 ч, превышая норму в 8-10 раз, и возвращается к норме на 3-5-й день заболевания. Выявлена прямая зависимость между степенью увеличения активности фермента и размерами зоны инфаркта.
В качестве критерия диагностики ОИМ АсАТ обладает низкой специфичностью, что объясняется его наличием и в других, органах: скелетных мышцах, почках, эритроцитах и др. Увеличение АсАТ при параллельном поражении этих органов может приводить к диагностическим ошибкам.
Неосложненный ОИМ, как правило, не приводит к увеличению АлАТ. Однако даже небольшое нарушение функции правого желудочка может привести к возникновению печеночной недостаточности и повышению уровня АлАТ.
Определение активности КФК и МВ-КФК
Активность КФКобщ и изофермента МВ-КФК на фоне ОИМ изменяется достаточно рано:
МВ-КФК обладает большей специфичностью в связи с преобладанием его активности именно в ткани миокарда. Степень увеличения КФК зависит от выраженности повреждения миокарда, локализации инфаркта и используемого метода определения.
Активность МВ-КФК была выявлена и в скелетной мускулатуре (3-4% общей активности), что делает некорректным определение этого фермента после проведения реанимационных процедур и оперативных вмешательств, на фоне шока, при воспалительных и дегенеративных мышечных заболеваниях, травматических поражениях, при интоксикации, делирии, гипотиреозе, остром психозе, у женщин непосредственно после родов.
Целесообразно также исследовать одновременно МВ-КФК и активность общей КФК и определять их процентное соотношение: (КФК-МВ/общая КФК) х 100%. При инфаркте миокарда это соотношение превышает 5-6%.
Определение ЛДГобщ и ЛДГ1,2
В типичных случаях активность ЛДГобщ увеличивается через 24-48 ч, достигает максимума к 3-6-му дню, превышая норму в 2-10.раз, и возвращается к исходному уровню на 8-14-й день заболевания в зависимости от тяжести повреждения миокарда.
Большую диагностическую значимость имеет определение ЛДГ1. Его активность начинает увеличиваться через 8-24 ч от начала заболевания, когда уровень ЛДГобщ еще не превышает норму. Активность ЛДГможет оставаться увеличенной и после того, как суммарная активность ЛДГ сыворотки уже возвращается к исходному уровню.
При небольших инфарктах активность ЛДГ1 может быть повышена, в то время как общая ЛДГ остается в пределах нормы.
Важным диагностическим критерием является также увеличение соотношения ЛДГ1/ЛДГ2. В норме оно составляет 0,45-0,74. У больных с ОИМ оно превышает 1,0. При исследовании гемолизированной сыворотки могут быть ложноположительные результаты, поскольку в кровь попадает большое количество ЛДГ1 из эритроцитов.
Определение уровня кардиспецифических тропонинов Т и I
В состав сократительного аппарата миоцитов входит тропониновый комплекс, образованный тремя белками: тропонином Т (ТрТ), образующим связь с тропомиозином, тропонином I, ингибирующим АТФ-ную активность, и тропонином С, обладающим значительным сродством к Са2+ Последний содержится также в скелетной мускулатуре. Содержание ТрТ в кардиомиоцитах примерно в два раза превышает уровень тропонина I. В крови здоровых людей даже после чрезмерной физической нагрузки уровень, тропонина Т нс превышает 0,2 — 0,5 нг/мл, поэтому возрастание его выше указанного предела свидетельствует о поражении сердечной мышцы. Специфичность этого маркера — 90 — 100%, что позволяет его считать «золотым» стандартом диагностики ОИМ.
Развитие инфаркта сопровождается обширным разрушением кардиомиоцитов и значительным выбросом в кровь ТрТ, уровень которого повышается в 20 — 40 раз. Увеличение ТрТ обнаруживается уже через 3-4 ч после начала болевого приступа. Максимальное повышение уровня ТрТ определяется на 3-4-е сутки, остается высоким в течение недели, а затем постепенно снижается, оставаясь повышенным до 10-18-го дня.
Определение тропонина I можно использовать в целях диагностики инфаркта миокарда у пациентов с сочетанным повреждением скелетных мышц. Показано, что острые и хронические повреждения скелетных мышц, чрезмерные физические нагрузки, хирургические операции, исключая операции на сердце, мышечные травмы не вызывают повышения уровня тропонина 1.
Определение миоглобина
Миоглобин — гемсодержащий хромопротеид, участвующий в транспорте кислорода в скелетных мышцах и миокарде.
Норма содержания миоглобина в крови составляет 12-52 нг/мл.
Определение миоглобина не является специфическим тестом. Однако повышение его в крови уже через 1-2 ч после ОИМ делает его самым ранним маркером ОИМ. Максимальные величины уровня миоглобина (превышение нормы в 4-15 раз) наблюдаются к 6-10 ч от начала заболевания. У пациентов с мелкоочаговым ОИМ уровень миоглобина приходит в норму через 24-36 ч, а при крупноочаговом ОИМ остается повышенным в течение 80 ч и более.
Повторное увеличение уровня миоглобина является достоверным показателем расширения зоны некроза или возникновения нового инфаркта миокарда.
Гипермиоглобинемия (более 900 нг/мл) в первые сутки заболевания является наиболее информативным показателем неблагоприятного исхода ОИМ.
Определение активности γ-глутамилтрансферазы(ГГТФ)
Динамика изменения активности этого фермента характеризует эффективность рубцевания некротизированной зоны миокарда. Нормализация активности фермента к 4-5-й неделе свидетельствует о завершении этого процесса и является хорошим прогностическим признаком.
Необходимо также исключить возможное повышение ГГТФ в результате алкогольной интоксикации, холестаза, цирроза печени, злокачественного новообразования печени или поджелудочной железы.
Определение активности ВВ-изофермента гликогенфосфортазы (GPBB)
.
Этот фермент катализирует перенос глюкозных остатков молекулы гликогена на неорганический фосфат с образованием глюкозофосфата. ВВ-изофермент найден в миокарде, его активность значительно увеличивается в первые 4 часа ОИМ. В связи с этим GPBB является одним из ранних маркеров его диагностики.
Определение концентрации малонового диальдегида
Используется для оценки степени выраженности ПОЛ и контроля эффективности антиоксидантной терапии. Интенсификация ПОЛ, являющаяся общим патобиохимическим симптомом повреждения клетки, происходит во всех случаях ОИМ. Постепенное снижение уровня малонового диальдегида у инфарктных больных на протяжении первых 10 дней заболевания является показателем благоприятного исхода ОИМ.
Помимо перечисленных тестов для контроля за течением заболевания и прогнозирования исхода применяется ряд показателей общего анализа крови, лейкоформулы, электролитов, коагулограммы, КЩР.
Определение количества лейкоцитов
Позволяет следить за динамикой течения ОИМ, выраженностью воспалительной реакции, определять наличие осложнений (эндокардит, перикардит, пневмония и др.). Количество лейкоцитов начинает нарастать через несколько часов и достигает максимума на 2-3-й день. При благоприятном течении ОИМ развивающийся лейкоцитоз (до 10-12х10^12/л) исчезает к концу первой недели заболевания.
СОЭ (скорость оседания эритроцитов) начинает увеличиваться на 2-3-й день, достигает максимальных Величин к 7-10 дню заболевания и нормализуется при полном замещении очага некроза соединительной тканью через 3-4 недели. Исчезновение лейкоцитоза с одновременным максимальным увеличением СОЭ на 7-10-й день называется симптомом «ножниц».
Уровень эозинофилов
Может увеличиваться на 2-й неделе ОИМ и часто является предвестником развития аутоиммунных процессов с формированием синдрома Дресслера.
Определение уровня калия, кальция
Определение уровня калия, кальция и показателей КЩР яроводится в первые трое суток ОИМ и далее — по показаниям. Гиперкалиемия (уровень калия выше 5,5 ммоль/л) опасна развитием AV-блокады, трепетания желудочков и остановкой сердца в диастоле.
Гипокалиемия (ниже 3,5 ммоль/л) может приводить к развитию тахикардии, аритмии и остановке сердца в систоле. Падение уровня кальция в крови больных ОИМ нередко предшествует летальному исходу.
По показаниям проводится определение показателей коагулограммы (АКТ, ПТИ, уровень тромбоцитов и их агрегация, паракоагуляционные тесты, Д-димер) для своевременной диагностики одного из опасных осложнений инфаркта миокарда — ДВС-синдрома. Уровень Д-димера используется для дифференциальной диагностики причины возникновения острой боли в груди. Его уровень менее 500 нг/мл исключает наличие у больного ТЭЛА.
Лабораторные признаки неблагоприятного прогноза ОИМ:
— лейкоцитоз выше 15×10^9/л, нейтрофилез с выраженным сдвигом влево;
— отсутствие снижения СОЭ после 10 дней;
— прогрессирующее увеличение концентрации сиаловых
кислот;
— устойчивый повышенный уровень С-реактивного белка и фибриногена;
— повторное появление в крови С-реактивного белка;
— повышение активности ферментов: АсАТ более 7 сут: ЛДГ более 2 недель; ЛДГ1,2 свыше 1 мес.; КФК более 7 сут, а также превышение нормы в 10 раз в 1-2 сут; КФК-МВ более 5 сут или увеличение более, чем в 20 раз по сравнению с нормой в первые сут; ГГТФ более 1,5 мес.; повторные гиперферментемии;
— гипермиоглобинемия более 5 суток или более 900 мкг/л в первые сутки;
— повторная гипермиоглобинемия;
— выраженный метаболический ацидоз (BE