Дефект межжелудочковой перегородки клинические рекомендации
Дефект межжелудочковой перегородки
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2018
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «18» апреля 2019 года
Протокол №62
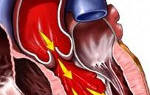
Дефект межжелудочковой перегородки – отверстие (или множественные отверстия) в перегородке между левым и правым желудочками
Название протокола: Дефект межжелудочковой перегородки
Код (-ы) МКБ-10:
Дата разработки/пересмотра протокола: 2013 год (пересмотр 2018 г.)
Сокращения, используемые в протоколе:
Пользователи протокола: детские кардиохирурги, детские кардиологи, интервенционные кардиологи, неонатологи, педиатры.
Категория пациентов: дети.
Шкала уровня доказательности:
Классификация
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез:
- одышка при нагрузке;
- частые легочные инфекции;
- симптомы прогрессирующей сердечной недостаточности;
- отставание в физическом развитии.
Физикальное обследование:
Внешний осмотр и пальпация: систолическое дрожание вдоль нижней половины левого края грудины. Деформация грудной клетки («сердечный горб») при больших ДМЖП и значительной дилатации ЛЖ.
Аускультация: у лиц c ЛГ отмечается значительное преобладание легочного компонента II тона, что определяется как акцент II тона в точке аускультации ЛА средней или высокой интенсивности (3-5/6) голосистолический или ранний систолический шум сброса крови через ДМЖП вдоль нижней половины левого края грудины. У пациентов с подартериальным ДМЖП может выслушиваться диастолический шум недостаточности аортального клапана из-за образования «грыжи» полулунных створок. У пациентов с ЛГ в проекции ЛА может выслушиваться диастолический шум гемодинамической недостаточности клапана ЛА на фоне ее выраженной дилатации (шум Грехема-Стилла).
Лабораторные исследования: повышенный уровень натрийуретического пропептида при наличии симптомов сердечной недостаточности (см. пункт 2.1.)
Инструментальные исследования:
- ЭКГ: гипертрофия ЛЖ, электрическая ось сердца.
- Обзорная рентгенография органов грудной клетки: тень сердца увеличена, удлинение сердечной тени в переднезадней проекции, имеет место центральное и периферическое усиление сосудистого рисунка легких, легочная артерия расширена.
- Эхокардиография: позволяет определить место дефекта и величину лево-правого шунта: перерыв изображения межжелудочковой перегородки, лево-правый (иногда право-левый) сброс крови при цветном допплеровском исследовании, дилатация ЛЖ, ПЖ различной степени, дилатация ЛА и межжелудочковый градиент.
- КТ-ангиография/МРТ: по показаниям для выявления сопутствующих ВПС.
Катетеризация полостей сердца: по показаниям для расчета гемодинамических параметров, определения операбельности.
Показания для консультации специалистов:
Показанием для консультации специалистов является наличие у пациента сопутствующих патологий других органов и систем за исключением ССС. Консультация может осуществляться как в до-, так и в послеоперационном периоде.
Диагностический алгоритм
Перечень основных диагностических мероприятий при госпитализации в стационар (пациент):
- Исследование на возбудителя сальмонеллеза, дизентерии, брюшного тифа
- Исследование кала на яйца гельминтов
- Консультация детского ЛОР-врача, детского стоматолога, детского кардиолога
- Рентгенография органов грудной клетки в одной проекции
- Мазок из зева на патфлору
- Микрореакция или реакция Вассермана (RW)
- HBsAg, антител к гепатиту В, С (ИФА)
- Исследование крови на ВИЧ
- Эхокардиография
- ЭКГ
- Общий анализ мочи
- Общий анализ крови (6 параметров)
- Определение общего белка, глюкозы, креатинина, мочевины, АлТ, АсТ – по показаниям
- ТТГ, Т3, Т4;
- при синдроме Дауна (трисомия по 21 хромосоме)
Перечень основных диагностических мероприятий при госпитализации в стационар (сопровождающее лицо):
- Исследование на возбудителя сальмонеллеза, дизентерии, брюшного тифа
- Исследование кала на яйца гельминтов
- Микрореакция или реакция Вассермана (RW)
- Флюорография
Основные диагностические мероприятия в стационаре:
Лабораторные исследования:
- Общий анализ мочи
- Общий анализ крови
- Биохимический анализ крови (определение общего белка, глюкозы, электролитов, АлТ, АсТ, С-реактивного белка, мочевины, креатинина, билирубина)
- Коагулограмма (протромбиновое время, фибриноген, фибриноген, МНО, АЧТВ, агрегация тромбоцитов)
- Определение группы крови и резус – фактора
- ЭКГ
- Эхокардиография (трансторакальная)
- Обзорная рентгенография органов грудной клетки
- Микробиологическое исследование (мазок из зева), чувствительность к антибиотикам
Дополнительные диагностические мероприятия в стационаре:
Лабораторные исследования:
Врожденные пороки сердца — клинические рекомендации
Врожденные пороки сердца (анатомические патологии самого органа либо его сосудов) составляют до 30% от всех врожденных болезней у взрослых пациентов и являются самыми распространенными из этой группы болезней. Формируются они внутриутробно на 2-8-й неделе беременности под действием на организм матери неблагополучных факторов (рентгеновское облучение, алкоголь, прием лекарств, перенесение краснухи, ветрянки, оспы, инфекции цитомегаловируса). Имеет значение и преемственная предрасположенность. Существует больше 100 видов ВПС. Побеседуем о наиболее часто встречающихся.
Классификация врожденных пороков
Дефект межпредсердной перегородки (ДМПП)
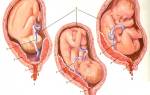
Один из самых распространенных врожденных пороков развития. Представляет собой сообщение между обоими предсердиями, ввиду чего происходит сброс артериальной крови из левого предсердия в правое (в норме такого быть не должно). Подлинный ДМПП прогрессирует при недоразвитии ткани. В период внутриутробного формирования между предсердиями есть отверстие — овальное окно, которое участвует в кровообращении плода, но уже после рождения в течение нескольких месяцев (до 1 года) оно должно зарасти. Если этого не происходит, формируется вторичный недостаток.
До 50% изъянов, локализующихся в области овального окна либо в аневризме межпредсердной перегородки, имеют тенденцию к спонтанному закрытию в 1-й год жизни. ДМПП иной локализации обыкновенно не закрываются и при маленьких размерах (5-6 мм) могут до 40-50 лет оставаться незамеченными, потому что их клинические проявления незначительны.
Пациентам с небольшими ДМПП и типичным размером правого желудочка традиционно не требуется медикаментозная терапия. Исключение составляют дети первых месяцев жизни с огромными ДМПП, сопровождающимися недостаточностью кровообращения. Операция показана при отсутствии склонности к закрытию недостатка и при возрастании степени нагрузки на правый желудочек. Сегодня множество ДМПП легко закрываются с применением чрескожного катетерного способа (не рекомендуется детям раннего возраста!).
Если процедура невыполнима по каким-то причинам, либо не подходит конкретному пациенту, возможно хирургическое закрытие выявленного дефекта заплатой либо его прямое ушивание. Отверстие, диаметр которого составляет менее 5 мм и без явных признаков перегрузки правого желудочка не отражается на продолжительность жизни ребенка (взрослого), следственно операция во многих случаях не требуется. При более выраженных (больших) дефектах с явлениями перегрузки их закрытие предпочтительно в детстве, ввиду того, что на третьей декаде жизни пациента разовьются клинические симптомы пороков.
Дефект межжелудочковой перегородки (ДМЖП)
Характеризуется наличием отверстия в перегородке сердца, через которое обогащенная кислородом кровь из левого желудочка может поступать в правый или наоборот. Бывает изолированным недостатком либо компонентом наиболее тяжелых пороков. До 80% таких отверстий самопроизвольно закрываются в 1-й месяц жизни. Различаются по месту расположения: под аортой, в среднем слое и мышечные.
Клинические проявления изолированного порока ДМЖП во многом зависят от размера дефекта ткани, а также степени тяжести легочной гипертензии (возрастания давления в артерии легких). При недостатках меньше чем 25% от диаметра отверстия аорты отсутствует перегрузка левого желудочка, дефекты более 25%, но менее 75% систематизируются как средние, характеризующиеся незначительной или умеренной перегрузкой сердца и гипертензией средней тяжести или без таковой. Симптомы, как правило ослабевают после медикаментозного лечения либо по прошествии определенного времени, потому что размер дефекта ДМЖП уменьшается самостоятельно или на фоне увеличения размера тела.
Если недостаток более чем 75% диаметра кольца аорты, имеет место перегрузка левого желудочка сердца и легочная гипертензия. Хирургическая операция при изолированном ДМЖП представляет собой локальное ушивание (при небольших дефектах), возможно закрытие «заплатой» (наиболее крупных дефектов). Пациенты, страдающие малыми видами ДМЖП без сопутствующих пороков развития, не нуждаются в ограничении физической активности. Впрочем, следует отказаться от непомерных нагрузок, путешествий в высокогорные районы, обезвоживания. Долгие авиаперелеты следует проходить с особой осторожностью.
Открытый артериальный проток (ОАП)
Такой порок сердца образует соустье между аортой и стволом легких, которое образуется в процессе внутриутробного оформления плода. Достаточно скоро после рождения (от нескольких часов до дней) проток закрывается. Если же он продолжает работать, это является врожденным пороком сердца, который проявляется непрерывным сбросом артериальной крови из большого — в малый круг кровообращения, в итоге которого перемешивается артериальная и венозная кровь в легких и прогрессирует перегрузка в малом круге кровообращения, что приводит к тяжелым патологическим изменениям в кровеносных сосудах легких и возникновению легочной гипертензии.
Врожденный дефект сердца может быть изолированным или сочетаться с другими формами пороков сердца (обычно с ДМЖП либо ДМПП). У большинства новорожденных с таким пороком сердца типичные симптомы могут отсутствовать. Среди старших неоперированных пациентов на уровне сердца выслушивается систолический шум, отслеживаются одышка и стремительная утомляемость . Больные с этим пороком, как правило, относятся к группе повышенной опасности по возможному появлению эндокардита, обструктивной, ярко выраженной легочно-сосудистой болезни и скоропостижной гибели!
Сегодня фактически всякий ОАП допустимо закрыть эндоваскулярно (операция под контролем рентгеноскопии). Противопоказаниями являются ранний детский возраст и маленькая масса тела. В этих случаях рекомендованы хирургическая перевязка либо наложение клипсы на проток. Закрытие ОАП показано многим взрослым сразу при обнаружении дефекта. Исключение — небольшие бессимптомные дефекты сердца без шума.
Коарктация аорты
Сужение либо полная закупорка просвета аорты на определенном участке, в результате которого сильно нарастает давление в ней и ее ветвях выше места сужения и понижается ниже него. То есть прогрессирует синдром артериальной гипертензии в сосудах головного мозга и верхней половины тела. Это ведет к перегрузке левого желудочка, гипертрофии миокарда с дальнейшей его дистрофией и присоединением со временем коронарной недостаточности .
Лечение только хирургическое! Безукоризненной операцией, исключительно у детей, является резекция (иссечение) суженного участка аорты. Но если она невыполнима при выраженной протяженности сужения и тяжелых изменениях стенки сосуда, проводится протезирование аорты и пластика места сужения заплатой.
Стеноз легочной артерии
Сужение артерии, при котором давление в правом желудочке возрастает, потому что его мышце нужно большее усилие, дабы протолкнуть кровь. Из-за этого нарушается каждый цикл работы сердца. Дети, у которых степень стеноза незначительная, могут прекрасно развиваться и отменно ощущать себя всю оставшуюся жизнь. У пациента с выраженной степенью стеноза в первые же дни вскоре после рождения возникает цианоз (голубой окрас кожи носогубного треугольника, ногтевых пластинок, синюшность губ) и стремительно прогрессирует недостаточность сердечно-сосудистой системы, не поддающаяся лечению.
Без операции половина таких детей гибнет на первом году жизни. Больные старшего возраста обычно предъявляют жалобы на одышку при физической нагрузке либо даже в покое. Множество бессимптомных пациентов не нуждаются в терапии. При наличии клинических проявлений назначается медикаментозное лечение.
Тетрада Фалло
Особенно часто регистрирующийся порок сердца так называемого синего типа. Состоит из четырех компонентов: сужения выходного отдела правого желудочка, высокого дефекта в области межжелудочковой перегородки, смещения устья аорты вправо (декстрапозиция) и гипертрофии миокарда правого желудочка.
Проявления порока во многом зависят от степени сужения легочной артерии. При выраженной наибольшая часть крови из правых отделов сердца попадает в левые, и в артериальной крови, которая разносится по организму, оказывается много не обогащенной кислородом венозной, имеющей наиболее темную окраску, чем и объясняется синюшность кожи. Если степень сужения незначительная, примесь венозной крови маленькая, цианоза может не быть. Некоторое время такой порок сердца может компенсироваться за счет гипертрофии мышцы сердца и увеличения числа эритроцитов в крови, что со временем может привести к повышенному риску образования тромбов.
Сразу после рождения ребенка признаки порока неприметны, поскольку в утробе он не мешает работе сердца. Через несколько дней (возможно недель) у младенца могут возникнуть синюшность кожи при кормлении и при плаче, одышка . Изредка цианоз проявляется только в то время, когда ребенок начинает ходить. Из-за нарушения кровоснабжения пальцы больного с возрастом приобретают вид барабанных палочек, ногти которых приобретают округлую форму в виде «часовых стекол». Пациенты сразу после нескольких незначительных движений требуют отдыха. Только 5% таких больных доживают до 40 лет без хирургического лечения. Тетрада Фалло — безусловное показание к операции!
Транспозиция магистральных сосудов
Один из самых тяжелых и распространенных (12-20% от всех встречающихся врожденных пороков сердца), которые сопровождаются цианозом тканей. Транспозицией именуется неправильное расположение основных сосудов, отходящих от сердца: аорта отходит не от левых, а от правых отделов, а легочная артерия — напротив. При полной транспозиции большой, а также малый круги кровообращения не сообщаются друг с другом, и в большом круге циркулирует не обогащенная кислородом венозная кровь.
Такое состояние несовместимо с жизнью, она зависит от наличия отверстия между предсердиями либо желудочками, через которое часть венозной крови может утекать в левые отделы и после этого в легкие — оба круга связаны между собой только этим шунтом. Дети с таким пороком рождаются значительно синюшными, они стремительно впадают в критическое коматозное состояние и, если им не оказать своевременную помощь, умирают в первые дни жизни.
Лечение оперативное: артериальное переключение — перемещение аорты и соединение ее со «своим» левым желудочком, а легочной артерии с правым. Наилучшее время для такой коррекции — 1-й месяц жизни. В совокупности итоги лечения приносят положительный результат. Сегодня сотни таких пациентов, подвергающихся хирургическому вмешательству, ведут активный образ жизни, а продолжительность жизни детишек, прооперированных одними из первых, обычно насчитывает 20 и больше лет.
Справочник по болезням (2012)
ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ
ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ
Дефект межжелудочковой перегородки (ДМЖП) — наличие сообщения между правыми и левыми камерами сердца. ДМЖП может рассматриваться как:
Самостоятельная патология врождённого генеза и относиться к группе врождённых пороков сердца (ВПС).
Составная часть комбинированного ВПС (тетрада Фалло, транспозиция магистральных сосудов, общий артериальный ствол, атрезия трёхстворчатого клапана и др.).
Распространённость ДМЖП — 1,5:1 000 живорождённых детей
Как осложнение ИМ — 1-3% случаев.
Врождённый характер (см. Тетрада Фалло)
Приобретённый характер — следствие ИМ.
Генетические аспекты. Многофакторная этиология. Имеются данные об аутосомно-доминантном и рецессивном наследовании.
В зависимости от анатомического расположения ДМЖП
выделяют дефекты перимембранозные, подартериальные отточные и мышечные.
Перимембранозные дефекты — дефекты соединительнотканной части межжелудочковой перегородки — наблюдают наиболее часто.
Подартериальные отточные дефекты располагаются в выходной части перегородки, которая практически отсутствует и представлена фиброзными кольцами, створками клапанов аорты и лёгочной артерии.
Мышечные дефекты — дефекты мышечной части межжелудочковой перегородки.
В зависимости от размера ДМЖП выделяют малые и большие дефекты.
Малые дефекты — болезнь Толочинова-Роже. Дефекты
имеют размер менее 1 см.
Большие дефекты — диаметр более 1 см или более 1/2 диаметра устья аорты.
В нормальных условиях в правом желудочке давление в период систолы в 4-5 раз ниже, чем в левом. При наличии ДМЖП происходит сброс крови слева направо.
При небольших дефектах сброс крови небольшой, давление в правом желудочке и лёгочных сосудах нормальное или незначительно повышено. Избыточное количество крови, поступающее через ДМЖП в малый круг, возвращается в левые отделы сердца, вызывая их перегрузку.
При больших дефектах большая часть крови из левого желудочка в момент систолы поступает в правый желудочек, что приводит к повышению давления в нём и сосудах малого круга кровообращения, формируя лёгочную гипертёнзию. Постепенно уменьшается величина сброса слева направо, давление в желудочках выравнивается. Увеличение лёгочного сопротивления приводит к сбросу крови справа налево. Такая картина характерна для синдрома Айзенменгера. Характерными признаками синдрома Айзенменгера считают отсутствие перегрузок левых отделов сердца, выраженную гипертрофию правого желудочка.
Малые дефекты (болезнь Толочинова-Роже)
Жалобы. Практически отсутствуют. В редких случаях симптомы небольшой утомляемости и одышки при нагрузке.
Физическое развитие не страдает
Слабо выраженный сердечный горб- непостоянный признак
Умеренно усиленный верхушечный толчок
Систолическое дрожание вдоль левого края грудины
Грубый систолический шум с максимумом в III-IV межреберьях
II тон заглушается систолическим шумом.
ЭКГ. Обычно в пределах возрастной нормы. В левых грудных отведениях могут отмечаться умеренные признаки перегрузки левого желудочка.
Рентгенологическое исследование органов грудной клетки
Размеры сердца нормальные или небольшое увеличение левого предсердия и желудочков 4 Талия сердца может быть сглажена
Лёгочной рисунок не усилен.
Эхокардиография. Визуализация дефекта.
Повышение насыщения крови кислородом в правом желудочке и лёгочной артерии
Давление в правых отделах слегка повышено
Лёгочное сопротивление нормальное
При рентгеноконтрастном исследовании хорошо виден сброс крови через небольшой дефект.
Жалобы зависят от степени выраженности недостаточности кровообращения
Одышка в покое или при физической нагрузке
Отставание в физическом развитии
Сердечный толчок усилен, разлитой
Систолическое дрожание слева от грудины и в области мечевидного отростка грудины
Застойные влажные хрипы в нижних отделах лёгких
I тон усилен на верхушке
II тон над лёгочной артерией резко акцентуирован и расщеплён
Систолический шум от пансистоличес-кого до короткого систолического, при одинаковом давлении в обоих желудочках шум может не прослушиваться
Диастолический шум на верхушке.
ЭКГ — признаки комбинированной гипертрофии обоих желудочков и предсердий; чаще отклонение ЭОС вправо
Рентгенологическое исследование органов грудной клетки
лёгочный рисунок усилен
сердце значительно увеличено
дуга лёгочного ствола выбухает по левому контору
Эхокардиография позволяет выявить прямые признаки дефекта, установить их количество, вариант и размеры, наличие лёгочной гипертёнзии
Катетеризация сердца необходима для определения выраженности сброса слева направо, лёгочно-сосудистого сопротивления и локализации дефектов. При большом ДМЖП отмечают повышение оксигенации и давления в правом желудочке и лёгочной артерии
Ангиокардиография позволяет судить о локализации дефекта, его размерах и исключить сопутствующую патологию.
Дифференциальная диагностика
Открытый общий АВ канал
Общий артериальный ствол
Дефект аортолёгочной перегородки
Отхождение магистральных сосудов от правого желудочка
Изолированный стеноз лёгочной артерии
Врождённая митральная недостаточность
Тактика ведения
Наблюдение в поликлинических условиях
Ограничение физической нагрузки
При появлении признаков недостаточности кровообращения (НК) необходимо назначение сердечных гликозидов
Госпитализация в случае тяжёлых застойных явлений, НК, ИМ. Лекарственная терапия. Включает лечение сердечной недостаточности, профилактику инфекционного эндокардита (см. Недостаточность сердечная, Эндокардит инфекционный).
Хирургическое лечение
При недостаточности кровообращения III степени для решения вопроса об операции необходимо проведение биопсии лёгкого (определение степени склерозирования лёгочных сосудов). При необратимых изменениях лёгочной ткани оперативное лечение противопоказано
Больные с малыми дефектами хирургическому лечению не подлежат
Паллиативное хирургическое лечение заключается в сужении лёгочной артерии на ограниченном участке для уменьшения сброса крови через дефект и снижения давления кровотока в лёгочной артерии
Радикальная коррекция. Закрытие ДМЖП — метод выбора независимо от возраста, массы тела, исходного состояния больного
Постинфарктный ДМЖП — устранение сброса крови и реваскуляризации миокарда с помощью аортокоронарного шунтирования.
Неэффективность консервативной терапии
Прогрессирующая лёгочная гипертёнзия.
Большие размеры дефекта с признаками значительного сброса
Частые респираторные заболевания
Отставание в физическом развитии
Желание проведения операции больным или его родителями.
Осложнения
Полная блокада сердца
Недостаточность трёхстворчатого клапана. Течение и прогноз
В 25-45% случаев ДМЖП закрывается спонтанно к 4-5-летнему возрасту
При небольших дефектах течение благоприятное
При больших дефектах течение тяжёлое и может привести к гибели в первые часы жизни. У 4% больных развивается инфекционный эндокардит.
Постинфарктный ДМЖП. Прогрессирующие лёгочно-сосудистые изменения утяжеляют прогноз; через 1 год при отсутствии хирургического лечения выживают 7% больных.
При постинфарктных ДМЖП составляет 15-50%
Госпитальная летальность при закрытии изолированных врождённых ДМЖП — менее 10%. Сопутствующая патология
Сочетание с аортальной недостаточностью (синдром Лобри-Пецци)
Дефект межжелудочковой перегородки у взрослых
Дефект межжелудочковой перегородки (ДМЖП) является наиболее распространенным врожденным пороком сердца и присутствует примерно у 3 — 4 младенцев из 1000 живорожденных детей. В результате спонтанного закрытия небольших дефектов межжелудочковой перегородки частота этого заболевания снижается с возрастом, особенно у взрослых. Большие ДМЖП, как правило, корригируются в детском возрасте. Без оперативного лечения у таких пациентов быстро развивается высокая легочная гипертензия, что делает их неоперабельными. Поэтому у взрослых пациентов чаще встречаются небольшие ДМЖП, либо сочетание ДМЖП со стенозом легочной артерии (ЛА), что ограничивает поступление крови в легкие и предотвращает развитие легочной гипертензии. Такие пациенты длительное время хорошо себя чувствуют, не предъявляют жалоб и не имеют ограничения физической активности и даже могут заниматься профессиональным спортом. Тем не менее, даже при относительно небольшом артериовенозном сбросе крови во взрослом возрасте ДМЖП может осложниться развитием аортальной недостаточности, аневризмой синуса Вальсальвы, инфекционным эндокардитом и другой кардиальной патологией.
Клиническая картина ДМЖП у взрослых пациентов типична для данного порока. При аускультации выслушивается систолический шум различной интенсивности слева и справа от грудины. Интенсивность шума зависит от размеров дефекта и степени легочной гипертензии. У больных с сопутствующей аортальной недостаточностью также выслушивается диастолический шум. При прорыве аневризмы синуса Вальсальвы шум носит «машинообразный» систолодиастолический характер. На ЭКГ выявляются признаки перегрузки левых отделов сердца за исключением пациентов со стенозом ЛА, когда преобладает нагрузка на правый желудочек (ПЖ). У пациентов с высокой легочной гипертензией (ЛГ) чаще наблюдается комбинированная гипертрофия желудочков, а при развитии синдрома Эйзенменгера – выраженная гипертрофия ПЖ (синдрома Эйзенменгера характеризуется развитием необратимой легочной гипертензии вследствие сброса крови слева направо).
Диагностика. Рентгенологическая картина представлена усилением легочного рисунка, а также увеличением тени сердца. У пациентов с малым ДМЖП рентгенография грудной клетки может быть нормальной. При наличии большого сброса крови слева направо имеются признаки увеличения левого предсердия, левого желудочка и усиление легочного рисунка. У пациентов с выраженной легочной гипертензией не будет увеличения левого желудочка (ЛЖ), но будет выбухание дуги легочной артерии и ослабление легочного рисунка на периферии легкого.
Допплер-эхокардиография является основным инструментальным методом современной диагностики ДМЖП, который позволяет получить достоверные данные об анатомии порока. Трансторакальная эхокардиография практически всегда имеет диагностическую ценность у большинства взрослых с хорошими эхокардиографическими окнами. Данные, которые нужно получить в ходе исследования, включают количество, размеры и локализацию дефектов, размеры камер, функцию желудочков, наличие или отсутствие аортальной регургитации стеноза легочной артерии, трехстворчатой регургитации. Оценка систолического давления в ПЖ также должна быть частью исследования. У взрослых с плохими эхокардиографическими окнами может потребоваться чреспищеводная эхокардиография.
Компьютерная томография с контрастным усилением и МР-томография могут применяться для оценки анатомии магистральных сосудов, если есть сопутствующие пороки, а также для визуализации тех ДМЖП, которые недостаточно хорошо видны на ЭхоКГ. Кроме того, МРТ позволяет оценить объем шунтирования крови, а также наличие фиброза в миокарде желудочков, который может развиваться в результате длительного существования порока.
Ангиокардиография и катетеризация сердца проводятся взрослым больным с ДМЖП, у которых неинвазивные данные не дают полной клинической картины. Согласно рекомендациям Американской ассоциации кардиологов, основные показания для этого исследования следующие:
-
определение объема шунтирования, а также оценка давления и сосудистого сопротивления малого круга кровообращения у пациентов с подозрением на легочную гипертензию;
обратимость легочной гипертензии должна быть проверена с помощью различных вазодилатирующих средств;
оценка сопутствующих пороков, таких как аортальная недостаточность, стеноз легочной артерии, прорыв аневризмы синуса Вальсальвы;
диагностика множественных ДМЖП;
выполнение коронароангиографии пациентам старше 40 лет с риском ИБС;
оценка анатомии ДМЖП в случаях, когда планируется эндоваскулярное его закрытие.
Хирургическое лечение. Согласно рекомендациям Американской ассоциации кардиологов, хирургическое закрытие ДМЖП необходимо при соотношении легочного кровотока к системному более чем 1,5:1,0. При сочетании ДМЖП со стенозом ЛА хирургическое лечение показано во всех случаях. Показанием к оперативному лечению является также прогрессирующая систолическая или диастолическая дисфункция ЛЖ, сопутствующая клапанная патология, прорыв аневризмы синуса Вальсальвы, инфекционный эндокардит в анамнезе.
Как правило, небольшие дефекты не приводят к развитию ЛГ, однако являются фактором риска развития инфекционного эндокардита, аортальной и трехстворчатой недостаточности и аритмий. Исходя из этого, C.Backer и соавт. (1993) рекомендуют хирургическое закрытие небольших перимембранозных ДМЖП как профилактику указанных осложнений. Следует отметить, что данный подход не является общепринятым, несмотря на достоверно высокую частоту развития сопутствующей кардиальной патологии у взрослых больных с ДМЖП.
Оперативное лечение ДМЖП выполняется в условиях искусственного кровообращения, гипотермии и кардиоплегии. Небольшие дефекты (до 5 — 6 мм) ушиваются, более крупные закрываются заплатой, обычно синтетическим материалом (например, дакроном, политетрафторэтиленом (Gore-Tex)). Доступ к ДМЖП осуществляется через правое предсердие, реже через правый желудочек. В случаях, когда одновременно выполняется протезирование аортального клапана, ДМЖП может закрываться доступом через аорту. Иногда при субтрикуспидальной локализации ДМЖП для визуализации его краев может потребоваться рассечение септальной створки трехстворчатого клапана с последующим ее восстановлением. В ряде случаев при удаленности краев перимембранозного ДМЖП от трехстворчатого и аортального клапанов, а также при мышечных ДМЖП возможно эндоваскулярное их закрытие при помощи специальных устройств (окклюдеров). Чрескожное закрытие ДМЖП представляет сбой привлекательную альтернативу хирургическому лечению у пациентов с высокими факторами риска оперативного вмешательства, неоднократными предшествующими хирургическими вмешательствами, плохо доступными мышечными ДМЖП и ДМЖП типа швейцарского сыра.
Противопоказанием к закрытию ДМЖП является склеротическая легочная гипертензия со сбросом крови справа налево (синдром Эйзенменгера). С целью улучшения качества жизни пациентам с синдромом Эйзенменгера показана легочная вазодилатационная терапия, включающая, в частности бозентан. Радикальным методом лечения является коррекция порока в сочетании с пересадкой легкого или пересадка сердечно-легочного комплекса. M. Inoue и соавт. (2010) сообщили об успешном закрытии ДМЖП с одновременной пересадкой обоих легких.
Основные принципы наблюдения пациентов с ДМЖП, оперированных во взрослом возрасте, сформулированы в Рекомендациях Американской ассоциации кардиологов (2008):
-
взрослые пациенты с ДМЖП и остаточной сердечной недостаточностью, резидуальным сбросом, легочной гипертензией, аортальной недостаточностью, обструкцией выводного тракта ПЖ и ЛЖ должны не реже одного раза в год проходить обследование;
взрослые пациенты с малыми остаточными ДМЖП и без какой-либо другой патологии должны обследоваться каждые 3 — 5 лет;
взрослые пациенты после закрытия ДМЖП окклюдером должны проходить обследование каждые 1 — 2 года в зависимости от локализации ДМЖП и других факторов;
пациентов, оперированных по поводу больших ДМЖП, следует наблюдать в течение всей жизни, так как в ряде случаев ЛГ может прогрессировать, кроме того, эти пациенты остаются в группе риска развития аритмий.
Взрослые без остаточного ДМЖП, без сопутствующих повреждений и с нормальным давлением в легочной артерии не нуждаются в продолжении наблюдения за исключением случаев направления на обследование врачом общей практики. Пациенты, у которых развивается бифасцикулярная блокада или транзиторная трифасцикулярная блокада после закрытия ДМЖП, имеют риск развития полной поперечной блокады сердца. Такие пациенты нуждаются в ежегодном обследовании.
Беременность пациентам с ДМЖП и тяжелой легочной гипертензией (комплекс Эйзенменгера) не рекомендуется из-за высокой материнской и внутриутробной смертности. Женщины с малыми ДМЖП без легочной гипертензии и без сопутствующих пороков не имеют большого сердечно-сосудистого риска при беременности. Обычно беременность хорошо переносится. Однако сброс крови слева направо может усилиться с увеличением сердечного выброса при беременности, это состояние уравновешивается снижением периферического сопротивления. У женщин с большим артериовенозным сбросом крови течение беременности может осложниться аритмиями, дисфункцией желудочков и прогрессированием легочной гипертензии.
Вопрос об обязательном хирургическом лечении взрослых пациентов с малыми ДМЖП, не имеющих осложнений, остается дискутабельным. Некоторые авторы считают, что тщательное наблюдение с целью ранней диагностики развивающихся осложнений является достаточным. Ключевыми моментами, которые должны отслеживаться у этих пациентов, являются развитие аортальной недостаточности, трехстворчатой регургитации, оценка степени шунтирования крови и легочной гипертензии, развитие желудочковой дисфункции, а также подлегочного и подаортального стенозов. Своевременное выполнение оперативного вмешательства позволит предотвратить дальнейшее прогрессирование кардиальной патологии. По мнению C. Backer и соавт. (1993), хирургическое лечение показано всем пациентам с теоретическим риском развития возможных осложнений ДМЖП.
Дефект межжелудочковой перегородки клинические рекомендации
Беременность у женщин с пороками сердца
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день.
Под пороком сердца понимают нарушения в его строении (различные дефекты клапана или стенок), которые могут вызывать сердечную недостаточность. Сердечная недостаточность — снижение способности сердца выполнять свою основную функцию — снабжать ткани и органы кровью. В результате организм испытывает недостаток кислорода. Все нарушения в строении сердца делятся на две большие группы:
- Можно ли планировать беременность с дефектом строения сердца
- Тонкости протекания беременности
- Особенности родов при дефектах сердца
- После родов расслабляться рано
- Важно знать будущей маме с пороком сердца
- Врожденные пороки сердца (ВПС) — дефект закладывается во внутриутробном периоде, страдают преимущественно стенки миокарда.
- Приобретенный порок сердца — дефект чаще всего касается строения клапанного аппарата сердца.
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Лечение зависит от способности сердца справляться со своими функциями. Если этого не происходит, то назначается хирургическая операция. При удачном исходе удается полностью восстановить функции сердца и избежать сердечной недостаточности.
Можно ли планировать беременность с дефектом строения сердца
По ряду физиологических причин, в том числе из-за увеличения объема крови на 25 – 50 %, сердце во время беременности работает на повышенных оборотах. Имея любой дефект строения сердца, об этом непозволительно забывать, планируя родить здорового ребенка и не подорвать собственное здоровье. Многие пороки сердца протекают бессимптомно, и человек может о них не знать, поэтому акушер-гинеколог наверняка направит на электрокардиограмму и УЗИ сердца.
Ответственно подходя к планированию беременности, девушка может обследовать состояние своего сердца самостоятельно еще до зачатия. Это особенно целесообразно при наличии любых жалоб со стороны сердечно-сосудистой системы:
- одышка;
- усиленное сердцебиение;
- повышенная утомляемость;
- отеки.
У подавляющего большинства людей (90 %) приобретенный порок сердца развивается как осложнение ревматизма, контроль состояния сердца особенно необходим для пациенток с этим диагнозом. Беременность при этом важно запланировать на период неактивного ревматического процесса.
Основным методом контроля состояния сердца служит УЗИ, вспомогательным — ЭКГ. Современная акушерская гинекология имеет в своем арсенале множество способов снизить риск беременности у женщины с пороком сердца.
Для этого есть два основных пути:
- Планирование оптимального времени зачатия — после оценки состояния пациентки дается рекомендация, в какой период лучше забеременеть.
- При незапланированной беременности врач может оценить риски и рекомендовать сохранить беременность или прервать ее.
После успешной операции на сердце женщине не рекомендуют беременеть в течение года, зато потом прогноз весьма благоприятный. Однако в каждом отдельном случае этот вопрос следует решать с врачом.
При ряде сложных патологий риск смерти матери крайне велик — 40 – 70 % случаев. Среди таких состояний:
- стеноз устья легочной артерии;
- тетрада Фалло;
- коарктация аорты;
- ряд других.
При таких состояниях врачи не рекомендуют беременеть и настаивают на прерывании уже существующей беременности. Беременность и пороки сердца могут быть совместимы, если не нарушается кровообращение. Но чем эти нарушения выражены сильнее, чем более активен ревматический процесс, тем больше риск для будущей матери и плода, который она вынашивает.
Тонкости протекания беременности
При врожденных дефектах в строении сердца течение беременности имеет свои особенности, следовательно, врач в каждом из таких случаев будет действовать особым образом, чтобы плод и будущая мама были в наибольшей безопасности.
Некоторые особенности беременности при девяти наиболее распространенных дефектах строения сердца отображены в таблице.
Дефект межпредсердной перегородки
Дефект межжелудочковой перегородки (ДМЖП)
Открытый артериальный проток
Стеноз клапана аорты
Стеноз клапана легочной артерии
Течение беременности и особенности родов при пороках сердца очень зависят от разновидности и выраженности патологии. Под угрозой оказывается не только сердце матери, но и детское сердечко и развитие.
Особенности родов при дефектах сердца
Особенность родов при пороке сердца у роженицы зависит от двух основных факторов:
- разновидности порока;
- степени компенсации особенностей сердечной деятельности перед родами.
Нередко необходимость отправиться в родильный зал у беременных с пороком наступает досрочно, чаще всего на 37 – 38 неделях. Так происходит из-за существенного возрастания нагрузки на сердце за несколько недель до предполагаемого срока рождения. К счастью, плод к этому моменту уже полностью сформирован и готов появиться на свет.
Родоразрешение может быть как естественным (в некоторых случаях без потуг), так и с помощью кесарева сечения. В планировании родов помимо акушера-гинеколога обязательно принимают участие реаниматолог и кардиолог.
После родов расслабляться рано
Роды — критический момент не только для детского, но и для материнского организма, многие привычные физиологические процессы после родов начинают протекать по-другому. На фоне этого проблемы сердечно-сосудистой системы могут обостряться. Снижение объема циркулирующей крови диктуют необходимость применения препаратов, поддерживающих работу сердца.
Грудное вскармливание возможно лишь в случае компенсированного порока сердца. Если же после родов мама должна принимать препараты, от ГВ придется отказаться, так как большинство лекарств могут навредить ребенку.
В первый год после родов велик риск обострения ревматизма, так что женщинам с этим диагнозом следует особенно тщательно наблюдать за своим состоянием.
Важно знать будущей маме с пороком сердца
Нередко беременности, для которых в принципе нет противопоказаний, несмотря на порок сердца будущей мамы, все-таки заканчиваются неблагоприятно. Так происходит из-за того, что женщины пускают на самотек свое состояние и протекание беременности — недостаточно посещают женскую консультацию, не обращаются к кардиологу.
Для этого нужно:
- тщательно планировать зачатие, не допускать случайностей;
- привлечь к планированию беременности кардиолога, заранее выяснить все возможные тонкости предстоящего периода;
- в случае врожденного порока сердца привлечь к планированию беременности специалиста-генетика, чтобы спрогнозировать вероятность наследования проблем с сердцем;
- соблюдение рекомендаций врача по поводу сна, питания, физической активности поможет выносить и родить здорового малыша;
- даже если кажется, что врачи требуют слишком часто их посещать и проходить слишком много диагностических процедур, порок сердца — то состояние, когда лучше проявить излишнюю бдительность, чем пропустить что-то важное.
Ребенок матери с пороком сердца нуждается в тщательном наблюдении в первые годы жизни, чтобы исключить различные патологии, например, открытое овальное окно, которое в некоторых случаях не зарастает после родов.
– оставляя комментарий, вы принимаете Пользовательское соглашение
- Аритмия
- Атеросклероз
- Варикоз
- Варикоцеле
- Вены
- Геморрой
- Гипертония
- Гипотония
- Диагностика
- Дистония
- Инсульт
- Инфаркт
- Ишемия
- Кровь
- Операции
- Сердце
- Сосуды
- Стенокардия
- Тахикардия
- Тромбоз и тромбофлебит
- Сердечный чай
- Гипертониум
- Браслет от давления
- Normalife
- Аллапинин
- Аспаркам
- Детралекс