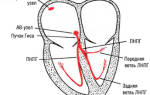
Вторичная недостаточность надпочечников
Надпочечниковая недостаточность
Что такое надпочечниковая недостаточность?
Надпочечниковая недостаточность (гипокортицизм) возникает, когда надпочечники не вырабатывают достаточное количество гормона кортизола. У человека есть два надпочечника и расположены они чуть выше почек. Надпочечники взаимодействуют с гипоталамусом и гипофизом головного мозга. Кортизол помогает расщеплять жиры, белки и углеводы в организме. Эти органы также контролируют артериальное давление и влияют на работу иммунной системы.
Надпочечниковая недостаточность может быть первичной, вторичной или третичной:
- Первичная недостаточность надпочечников. Она известна как болезнь Аддисона. Возникает, если надпочечники повреждены и не производят достаточно гормонов кортизола и альдостерона. Такое состояние встречается редко, однако возникнуть может в любом возрасте.
- Вторичная надпочечниковая недостаточность. Данный тип недостаточности начинается, когда гипофиз не производит достаточного количества гормона АКТГ (адренокортикотропин). В результате надпочечники не вырабатывают достаточного количества кортизола.
- Третичная надпочечниковая недостаточность. Она появляется в результате, когда гипоталамус не производит достаточного количества кортикотропин-рилизинг-гормона (или кортикотропин-рилизинг-фактор, сокращённо КРГ). В результате гипофиз не производит достаточно гормона АКТГ.
Что вызывает надпочечниковую недостаточность?
Первичная недостаточность надпочечников чаще всего возникает, когда иммунная система нападает на здоровые клетки надпочечников по ошибке, воспринимая их чужеродными. Другие причины могут включать:
- рак надпочечников;
- грибковая инфекция;
- туберкулезная инфекция надпочечников;
- наследственные нарушения эндокринных желез.
Недостаток адренокортикотропного гормона (АКТГ и другие названия: кортикотропин, адренокортикотропин, кортикотропный гормон) приводит к вторичной надпочечниковой недостаточности. Это может произойти, если больной принимает определенные синтетические глюкокортикоидны в течение длительного времени из-за проблем со здоровьем. Например, людям с астмой или ревматоидным артритом может потребоваться долгий прием преднизолона. Другие причины включают:
- опухоли гипофиза (как доброкачественные, так и злокачественные);
- потеря кровотока в гипофизе;
- гипофиз удален или проводилась лучевая терапия гипофиза при лечении опухолей;
- удалены части гипоталамуса.
Симптомы надпочечниковой недостаточности
У больного могут быть слабовыраженные симптомы и признаки, если он находится в состоянии физического стресса. Симптомы у каждого человека будут разными. Человек может испытывать следующие признаки:
- слабость;
- усталость и недостаток энергии (апатия);
- головокружение;
- темная кожа, часто на лице, шее и тыльной стороне рук (только при болезни Аддисона);
- голубовато-черный цвет вокруг сосков, рта, прямой кишки, мошонки, влагалища или других мест (только при болезни Аддисона);
- потеря веса;
- потеря жидкости (обезвоживание);
- отсутствие аппетита;
- боль в мышцах;
- расстройство желудка (тошнота);
- рвота;
- понос;
- низкое кровяное давление;
- низкий уровень сахара;
- у женщин нерегулярные или отсутствие менструации.
Если не лечить, надпочечниковая недостаточность может осложниться и привести к:
- cильным болям в животе;
- крайней слабости;
- низкому кровяному давлению;
- почечной недостаточности;
- шоку.
Эти симптомы могут выглядеть как другие проблемы со здоровьем. Всегда обращайтесь к врачу для постановки диагноза.
Диагностика надпочечниковой недостаточности
Лечащий врач спросит о вашей истории болезни. Вам также понадобится сдать анализы. Тесты, которые могут диагностировать надпочечниковую недостаточность, включают:
- Анализы крови, мочи или слюны. Они могут показать уровень гормонов надпочечников и АКТГ, а также могут показать изменения уровня натрия и калия в крови.
- Визуальные исследования. К ним относятся рентгенография, ультразвуковое исследование и МРТ.
Лечение надпочечниковой недостаточности
Лечение будет зависеть от симптомов, возраста и общего состояния здоровья. Терапия также будет зависеть от того, насколько серьезным является состояние.
Вам нужно будет принимать гормоны, чтобы заменить те, которые не вырабатываются надпочечниками, в основном кортизол.
Болезнь Аддисона может быть смертельной. Лечение часто начинается с видения внутривенных жидкостей и лекарств, называемых кортикостероидами. Больной может принимать эти лекарства перорально или в/в. Возможно, больному придется принять их всю оставшуюся жизнь.
Пациенту также может потребоваться принимать другие лекарства (флудрокортизоны). Это может помочь поддерживать нормальный уровень натрия и калия в организме.
Каковы возможные осложнения надпочечниковой недостаточности?
У человека могут быть внезапные серьезные симптомы. Это называется острой надпочечниковой недостаточностью или аддисоновским кризисом. Она может произойти, когда тело находится в состоянии стресса. Состояние может возникнуть по многим причинам, таким как болезнь, лихорадка, операция или обезвоживание.
Также может возникнуть кризис, если вы прекратите прием кортикостероидов или резко снизите количество лекарств. Симптомы аддисоновского кризиса включают те же симптомы надпочечниковой недостаточности или болезни Аддисона. Если аддисоновский кризис не лечится, он может привести к:
Жизнь с надпочечниковой недостаточностью
Больной должен принимать лекарства, как предписано врачом. Также люди с надпочечниковой недостаточностью должны всегда иметь при себе медицинскую карту или спец. бирку, которая может гарантировать, что человек получит правильное лечение в случае крайней необходимости.
Во время путешествий всегда носите с собой запасной комплект кортизола.
Когда следует звонить своему врачу?
Любое состояние, которое вызывает стресс вашего тела, может повлиять на то, сколько лекарств вам нужно. Позвоните своему врачу, если:
- У вас есть какие-либо заболевания, особенно лихорадка, рвота или диарея.
- Вы забеременели.
- Вам нужна операция.
Немедленно обратитесь за медицинской помощью, если у вас появятся внезапные тяжелые симптомы (аддисоновский кризис).
Ключевые моменты о надпочечниковой недостаточности (болезнь Аддисона)
- Надпочечниковая недостаточность возникает, когда надпочечники не вырабатывают достаточное количество гормона кортизола. Есть 3 типа этого расстройства.
- Основной тип известен как болезнь Аддисона. Возникает редко, когда надпочечники не вырабатывают достаточное количество гормонов кортизола и альдостерона.
- Вторичный тип возникает, когда гипофиз не вырабатывает достаточное количество гормона АКТГ. Надпочечники тогда не производят достаточно кортизола.
- Третичный тип возникает, когда гипоталамус не производит достаточного количества кортикотропин-рилизинг-гормона. Тогда гипофиз не производит достаточно АКТГ.
- Легкие симптомы могут быть видны только тогда, когда человек находится в состоянии физического стресса. Другие симптомы могут включать слабость, усталость и недостаток энергии, а также потерю веса.
- Больному нужно будет принимать гормоны, чтобы заменить те, которые надпочечники не вырабатывают.
Прогноз варьируется в зависимости от различных этиологий, но, как правило, коррелирует с быстрой диагностикой и медицинской помощью. Летальных исход — это редкое явление, когда пациенты получают адекватную медицинскую помощь.
Заключение
Надпочечниковая недостаточность — это сложный и многофакторный синдром, который в клинической практике может быть трудно диагностирован, особенно в экстренных ситуациях и врачами-неспециалистами. Для обеспечения оптимального диагностическо-терапевтического подхода необходимо уделять большое внимание признакам и симптомам, зачастую неспецифическим, а иногда и недооцениваемым. Имеющиеся данные подчеркивают важность стандартизированного подхода для осознанного и надлежащего лечения, особенно детей, страдающих надпочечниковой недостаточностью.
Для предупреждения надпочечникового криза необходимо проведение адекватной заместительной гормональной терапии при хронической недостаточности коры надпочечников и других заболеваниях, требующих постоянного приема кортикостероидов.
Ни в коем случае нельзя самостоятельно прекращать приём кортикостероидов или снижать их дозировку. Необходимо постоянно поддерживать контакт с врачом-эндокринологом, который корректирует дозу лекарства в зависимости от физической активности и состояния здоровья пациента.
Надпочечниковая недостаточность
Под этим названием объединяют болезни, вызванные гипофункцией коры надпочечников. Клинические проявления надпочечниковой недостаточности обусловлены дефицитом глюкокортикоидов и (реже) дефицитом минералокортикоидов.
Этиология и классификация
А. Первичная надпочечниковая недостаточность (болезнь Аддисона) — это следствие первичного заболевания надпочечников, при котором разрушается более 90% клеток коркового вещества, секретирующих кортикостероиды.
Б. Вторичная надпочечниковая недостаточность обусловлена заболеваниями гипоталамуса или гипофиза, приводящими к дефициту кортиколиберина или АКТГ (или и того, и другого гормона одновременно).
В. Ятрогенная надпочечниковая недостаточность возникает при прекращении глюкокортикоидной терапии или быстром падении уровня эндогенных глюкокортикоидов на фоне длительного угнетения гипоталамо-гипофизарно-надпочечниковой системы экзогенными или эндогенными глюкокортикоидами.
Г. Надпочечниковая недостаточность может быть острой и хронической. Причины острой надпочечниковой недостаточности: быстрое разрушение коры надпочечников (например, при двустороннем кровоизлиянии в надпочечники), повреждение надпочечников при травме или хирургическом вмешательстве.
Хроническая надпочечниковая недостаточность
А. Этиология. Хроническая надпочечниковая недостаточность может быть первичной и вторичной; клиническая картина в этих случаях несколько различается. В последнее время самой распространенной причиной первичной надпочечниковой недостаточности является аутоиммунное поражение коры надпочечников (примерно 80% случаев). Аутоиммунное поражение надпочечников может сопровождаться другими аутоиммунными эндокринными заболеваниями, например инсулинозависимым сахарным диабетом и гипотиреозом, а иногда и гипогонадизмом, гипопаратиреозом и аутоиммунным гастритом (аутоиммунный полигландулярный синдром типа I). В первой половине XX века ведущей причиной хронической первичной надпочечниковой недостаточности был туберкулез. В наши дни только 10—20% случаев первичной надпочечниковой недостаточности обусловлены туберкулезным поражением надпочечников.
Б. Клиническая картина
1. Симптомы, общие для первичной и вторичной надпочечниковой недостаточности, обусловлены в первую очередь дефицитом глюкокортикоидов и включают утомляемость, слабость, гипогликемию, потерю веса и желудочно-кишечные нарушения. При первичной надпочечниковой недостаточности поражаются и клетки клубочковой зоны коры надпочечников, секретирующие минералокортикоиды, что приводит к гипоальдостеронизму. Симптомы гипоальдостеронизма: потеря натрия, повышенное потребление соли, гиповолемия, артериальная гипотония, гиперкалиемия, легкий метаболический ацидоз. Поскольку при первичной надпочечниковой недостаточности гипофиз не повреждается, дефицит кортизола вызывает компенсаторное повышение секреции АКТГ и МСГ , что приводит к гиперпигментации кожи и слизистых. Гиперпигментация чаще всего заметна вокруг губ и на слизистой щек, а также на открытых или подвергающихся трению частях тела. При аутоиммунном поражении надпочечников могут одновременно наблюдаться множественные веснушки, разлитая гиперпигментация и витилиго. Секреция андрогенов также снижается, что приводит к уменьшению подмышечного и лобкового оволосения.
2. Вторичная надпочечниковая недостаточность не сопровождается гипоальдостеронизмом, поскольку синтез минералокортикоидов контролируется не АКТГ , а ренин-ангиотензиновой системой. Нет и гиперпигментации, поскольку уровни АКТГ и МСГ снижены. Важный признак вторичной надпочечниковой недостаточности — сопутствующие патологии, обусловленные дефицитом ЛГ и ФСГ , ТТГ или СТГ (соответственно вторичный гипогонадизм, вторичный гипотиреоз и задержка роста).
Гипоадреналовый криз (острая надпочечниковая недостаточность)
А. Этиология. Тяжелые инфекции, прием метирапона , травма или хирургическое вмешательство у больных с хронической надпочечниковой недостаточностью могут спровоцировать гипоадреналовый криз.
Б. Клиническая картина. Высокая лихорадка, дегидратация, тошнота, рвота и падение АД , которое быстро приводит к обмороку. При дефиците минералокортикоидов наблюдаются гиперкалиемия и гипонатриемия. Дегидратация приводит к повышению АМК и (не всегда) к гиперкальциемии. Гипоадреналовый криз может быть вызван двусторонним кровоизлиянием в надпочечники, например при передозировке гепарина .
Ятрогенная надпочечниковая недостаточность. Длительное лечение глюкокортикоидами угнетает гипоталамо-гипофизарно-надпочечниковую систему. Устойчивость этой системы к экзогенным глюкокортикоидам у разных больных неодинакова. Обычные симптомы угнетения гипоталамо-гипофизарно-надпочечниковой системы после отмены глюкокортикоидной терапии: слабость, утомляемость, депрессия, артериальная гипотония. При тяжелом стрессе, если вовремя не увеличить дозу глюкокортикоидов, у больного может развиться гипоадреналовый криз. Угнетение гипоталамо-гипофизарно-надпочечниковой системы иногда проявляется резкой слабостью во время или после незначительных стрессов или недомоганий, например при респираторных заболеваниях. Клинические симптомы могут отсутствовать, и только биохимические сдвиги (например, сниженная секреция кортизола в пробах с АКТГ ) свидетельствуют о недостаточности гипоталамо-гипофизарно-надпочечниковой системы. Ятрогенную надпочечниковую недостаточность следует заподозрить в следующих случаях:
А. У любого больного, получавшего преднизон в дозе 15—30 мг/сут на протяжении 3—4 нед. У таких больных после отмены глюкокортикоидной терапии угнетение гипоталамо-гипофизарно-надпочечниковой системы может сохраняться в течение 8—12 мес.
Б. У любого больного, получавшего преднизон в дозе 12,5 мг/сут на протяжении 4 нед. Угнетение гипоталамо-гипофизарно-надпочечниковой системы может сохраняться в течение 1—4 мес.
В. У любого больного с синдромом Кушинга после удаления аденомы или злокачественного новообразования надпочечника.
Г. У любого больного со снижением секреции кортизола в ответ на АКТГ , получающего глюкокортикоиды (независимо от дозы и продолжительности глюкокортикоидной терапии).
Лабораторная диагностика
А. Короткая проба с АКТГ . Используют синтетический аналог АКТГ — тетракозактид — мощный и быстродействующий стимулятор секреции кортизола и альдостерона. Пробу можно проводить в стационаре или амбулаторно, причем ни время суток, ни прием пищи не влияют на точность результатов.
а. Берут кровь для определения базальных уровней кортизола и альдостерона в сыворотке и АКТГ в плазме. Определение альдостерона и АКТГ помогает отличить первичную надпочечниковую недостаточность от вторичной.
б. В/в или в/м вводят 0,25 мг тетракозактида . Для в/в введения тетракозактид разводят в 2—5 мл физиологического раствора; продолжительность инфузии — 2 мин.
в. Через 30 и 60 мин после введения тетракозактида берут кровь для определения уровней кортизола (и при необходимости — альдостерона и АКТГ ).
2. Оценка результатов. В норме уровень кортизола после введения тетракозактида повышается не менее чем на 10 мкг%. Если базальная концентрация кортизола превышала 20 мкг%, результаты пробы недостоверны. Нормальная секреторная реакция позволяет с уверенностью исключить первичную надпочечниковую недостаточность. У больных со вторичной надпочечниковой недостаточностью реакция на тетракозактид обычно снижена, но иногда бывает нормальной. Первичную надпочечниковую недостаточность можно отличить от вторичной, измерив базальный уровень АКТГ и уровень альдостерона до и после введения тетракозактида . При первичной надпочечниковой недостаточности базальный уровень АКТГ повышен (обычно > 250 пг/мл), тогда как при вторичной он снижен или находится в пределах нормы. При первичной надпочечниковой недостаточности базальный уровень альдостерона снижен, а после введения тетракозактида секреция альдостерона не усиливается. При вторичной надпочечниковой недостаточности базальный уровень альдостерона в пределах нормы или снижен, но через 30 мин после введения тетракозактида концентрация альдостерона возрастает не менее чем на 111 пмоль/л.
Если секреторная реакция надпочечников на АКТГ не нарушена, но имеются клинические признаки вторичной надпочечниковой недостаточности, используют другие пробы, которые позволяют выявить снижение резерва АКТГ (например, пробы с метирапоном ).
Б. Короткая проба с метирапоно м
1. Цель: установить или подтвердить диагноз надпочечниковой недостаточности. Проба особенно полезна, когда есть основания подозревать вторичную надпочечниковую недостаточность. Метирапон — это ингибитор 11бета-гидроксилазы — фермента коры надпочечников, превращающего 11-дезоксикортизол в кортизол. Снижение уровня кортизола после введения метирапона стимулирует секрецию АКТГ , который активирует синтез глюкокортикоидов. Поскольку конечный этап синтеза кортизола блокирован метирапоном , происходит накопление непосредственного предшественника кортизола — 11-дезоксикортизола. Последний не подавляет секрецию АКТГ по принципу обратной связи, и потому уровни АКТГ и 11-дезоксикортизола продолжают повышаться. Измеряют концентрацию 11-дезоксикортизола в сыворотке или в моче (где он присутствует в виде тетрагидро-11-дезоксикортизола). Определение 11-дезоксикортизола в сыворотке — более чувствительный метод, поскольку содержание этого метаболита в крови возрастает в гораздо большей степени, чем в моче.
а. Метирапон дают внутрь в 24:00. При весе 90 кг — 3 г. Препарат принимают с едой, чтобы уменьшить тошноту.
б. На следующее утро в 8:00 определяют содержание кортизола и 11-дезоксикортизола в сыворотке.
3. Оценка результатов. В норме концентрация 11-дезоксикортизола после введения метирапона должна превышать 7,5 мкг%. При первичной или вторичной надпочечниковой недостаточности концентрация 11-дезоксикортизола не достигает 5 мкг%. Метирапоновая блокада считается полной при концентрации кортизола 20 мкг% указывают на полное восстановление функции гипоталамо-гипофизарно-надпочечниковой системы. Если уровень кортизола в 8:00 > 10 мкг%, но реакция на АКТГ снижена, то при тяжелых сопутствующих заболеваниях могут вновь потребоваться экзогенные глюкокортикоиды. Эта потребность будет сохраняться до тех пор, пока секреторная реакция надпочечников на АКТГ не нормализуется.
Источник: Н.Лавин «Эндокринология», пер. с англ. В.И.Кандрор, Москва, «Практика», 1999
опубликовано 09/09/2011 13:16
обновлено 31/07/2013
— Болезни коры надпочечников
Вторичная недостаточность надпочечников
Кортикостерон и 11-дезоксикортикостерон.
Вирильный синдром при ВДКН. Вирилизация наружных половых органов у плода женского пола при ВДКН происходит вследствие повышенной продукции надпочечниками андрогенов при недостаточности ферментов, которые принимают участие только в биосинтезе глюко- и минералокортикоидов. При постоянно повышенном уровне АКТГ и гиперстимуляции надпочечников в них происходит накопление промежуточных соединений, в частности 17-ОН-прогестерона, а активация вторичных путей их метаболизма (основные блокированы) усиливает образование андростендиона и тестостерона. Этому способствует и гиперплазия надпочечников. Как указывалось выше, гипоталамо-гипофизарно-надпочечниковая система начинает функционировать на 10-12 неделе беременности. С 10-й недели происходит также формирование наружных половых органов плода, а повышенное образование андрогенов в надпочечниках нарушает этот процесс. Происходит вирилизация или андрогенизация наружных половых органов плода. Классическими формами ВДКН с вирильным синдромом являются 21- и 11-гидроксилазная недостаточность.
Синдром потери соли при ВДКН. Он развивается в результате недостаточной продукции альдостерона при дефекте ферментов 3β-гидроксистероиддегидрогеназы и полном блоке 21-гидроксилазы. При этом развивается гипонатриемия, гиперкалиемия и обезвоживание. Описан и вариант недостаточного биосинтеза альдостерона при дефекте 18-дегидрогеназы, последнего фермента по пути биосинтеза этого гормона, при этом другие проявления ВДКН, характерные для остальных его вариантов, отсутствуют.
Синдром артериальной гипертензии. Он характерен для 11-гидроксилазной недостаточности, которая развивается вследствие дефекта кофермента Р450с11, в результате чего в надпочечниках происходит накопление дезоксикортикостерона, который хоть и является промежуточным соединением на пути биосинтеза альдостерона, уже обладает высокой минералокортикоидной активностью. Артериальная гипертензия отмечается и при недостаточности Р450с17 и дефекте фермента 17α-гидроксилазы и блокирования 17-гидроксилирования прогестерона.
Синдром неполной маскулинизации. Развивается у мальчиков с вариантами ВДКН, которые обусловлены недостаточностью ферментов, участвующих в биосинтезе тестостерона. Формирование наружных половых органов у плода мужского пола происходит нормально только при условии достаточной продукции андрогенов тестикулами, что предполагает сочетанный ферментативный дефект и в них. Была продемонстрирована недостаточность 3β-гидроксистероиддегидрогеназы одновременно в надпочечниках и тестикулах, что предполагает общий генетический контроль биосинтеза тестостерона в этих железах внутренней секреции.
Синдром липоидной гиперплазии. Этот синдром обусловлен двойным дефектом: 1) нарушением стероидогенеза вследствие генетической мутации СТАР-протеина; 2) повреждением клеток за счёт накопления в митохондриях эфиров холестерина. Вследствие полного блока биосинтеза андрогенов (по-видимому, как в надпочечниках, так и в ткани тестикул) наружные половые органы плода обоего пола под влиянием автономной тенденции к феминизации формируются по женскому типу.
Классификация и клиническая картина.
В настоящее время выделяют три основные формы ВДКН, которые составляют более 90% всех случаев болезни:
Простая, вирильная или компенсированная форма. Она обусловлена частичной недостаточностью 21-гидроксилазы. Единственным клиническим признаком болезни при рождении является неправильное строение наружных половых органов.
У мальчиков наружные половые органы сформированы в целом правильно, по мужскому типу, но с различной степенью выраженности макрогенитосомии (увеличения размеров) и пигментации. При незначительной выраженности этих изменений в периоде новорождённости их могут не заметить.
У девочек наружные половые органы сформированы неправильно, с различной степенью выраженности вирилизацией. При лёгкой степени вирилизации отмечается только гипертрофия клитора, его форма не изменена и в ряде случаев эти изменения у новорождённых девочек не замечают. При более выраженной средней степени вирилизации (наблюдается наиболее часто) выявляется гермафродитное строение гениталий: клитор не только гипертрофирован, но и становится пенисообразным, формируется головка и крайняя плоть; уретра открывается одним отверстием с влагалищем, формируя sinus urogenitalis с узким воронкообразным входом во влагалище; малые половые губы гипоплазированы, большие половые губы становятся складчатыми и пигментированными. В более редких случаях при значительной вирилизации большие половые губы могут срастаться, напоминая расщеплённую мошонку; клитор с пенильной уретрой; может отмечаться атрезия наружных двух третей влагалища.
Тяжёлая, сольтеряющая форма. Эта форма обусловлена полным блоком 21-гидроксилазы. Изменения наружных половых органов идентичны простой вирильной форме. Если диагноз при рождении не был поставлен, то самое раннее на 2-3 сутки, иногда в течение первых 2-х недель после рождения появляется рвота фонтаном, жидкий стул, признаки дегидратации с последующим развитием коллапса или шока – развивается острая надпочечниковая недостаточность. Необходима неотложная посиндромная терапия.
Гипертоническая или гипертензивная форма. В основе её развития лежит недостаточность 11α-гидроксилазы. Клинически эта форма полностью идентична простой или вирильной, но сопровождается и артериальной гипертензией.
Редкие формы ВДКН. В случае несоответствия строения наружных половых органов генотипу новорождённого (при генотипе 46XY строение гениталий женского типа) помимо других вариантов нарушения половой дифференцировки необходимо исключить и такие формы ВДКН, как врождённая липоидная гиперплазия и недостаточность 17-гидроксилазы.
Пренатальная диагностика стала возможной благодаря развитию техники молекулярно-генетических исследований, но ещё не вошла в широкую медицинскую практику и пока носит экспериментальный характер. При этом путём амниоцентеза в клетках амниотической жидкости или в пробах ворсинок хориона определяют возможность мутации Р450с21, в самой амниотической жидкости определяют уровень не только 17-ОН-прогестерона, но и других метаболитов. Родителей пробанда обследуют с нагрузкой препаратами АКТГ для исключения гетерозиготных носителей.
Диагноз надпочечниковой недостаточности.
Диагноз острой надпочечниковой недостаточности, в том числе и в периоде новорождённости нередко ставится на основании анамнеза и клинических данных, т.к. необходимо, как правило, неотложное проведение посиндромной терапии по витальным показаниям не дожидаясь лабораторных данных.
Развитие надпочечниковой недостаточности вероятно у любого остро заболевшего ребёнка с явлениями шока, периферического коллапса с частым пульсом слабого наполнения, у детей с признаками недостаточного питания, отстающих в развитии, с гипертермией, гипогликемией и судорогами. Характерна также гиперпигментация в области разгибательных и крупных складок, наружных половых органов, по белой линии живота, ареол. Гипонатриемия и гиперкалиемия по данным экспресс-анализа электролитов характерны для минералокортикоидной недостаточности, изолированная гипонатриемия может быть одним из проявлений глюкокортикоидной недостаточности.
Неправильное, а тем более гермафродитное строение гениталий всегда должно являться поводом для исключения различных вариантов ВДКН.
При проведении исследования гормонального профиля необходимо помнить о том, что и у здоровых новорождённых уровень кортизола низкий и не имеет ещё характерных для более старшего возраста суточных колебаний, поэтому его лучше определять с использованием нагрузочных проб. Для этого используют 1-часовой нагрузочный тест с АКТГ с последующим капельным введением глюкокортикоидов, солевых растворов. При первичной надпочечниковой недостаточности, включая ВДКН, нагрузочные тесты не требуются, т.к. уже исходный уровень АКТГ в крови резко повышен.
Для уточнения характера ферментативного дефекта и уточнения диагноза проводят исследование различных промежуточных метаболитов биосинтеза стероидов корой надпочечников. Скринингом (и диагностическим маркёром одновременно) наиболее часто встречающихся форм ВДКН является определение в крови новорождённого повышенного уровня 17-ОН-прогестерона, что характерно для недостаточности 21-гидроксилазы, независимо от степени её выраженности. С учётом особенностей клинических проявлений и строения наружных половых органов необходимо помнить, что повышенный уровень 17-ОН-прогестерона может также отмечаться при недостаточности 11-гидроксилазы, а его значительное повышение выявляется также и при дефиците 3β-гидрокси-стероиддегидрогеназы.
Лечение надпочечниковой недостаточности.
У новорождённых в критическом состоянии необходимо проведение неотложной посиндромной терапии, но, при возможности, до введения гормональных препаратов желательно взять пробу крови для уточнения диагноза.
В случае гиповолемии и дегидратации начинают внутривенное введение физиологического раствора в 5% глюкозе 100-120 мл/кг в течение первых 24 часов. При шоке показано введение плазмы или 5% альбумина 10-20 мл/кг. Одновременно начинают заместительную гормональную терапию и препаратом выбора является гидрокортизон гемисукцинат или фосфонат, 1.5-2 мг/кг вводят немедленно внутривенно, а затем налаживают постоянное внутривенное введение препарата 30 мг/м 2 /сутки. При невозможности внутривенного введения, гидрокортизон гемисукцинат вводится в/м по 2 мг/кг по мере необходимости.
Для последующей долговременной заместительной терапии используют гидрокортизон или кортизон ацетат 10-12 мг/м 2 /сутки. Кортизон ацетат можно также вводить внутримышечно каждые 3 дня, но этот режим используется редко. В случае какой-либо стрессовой ситуации кортизон ацетат вводится в дозе 30 мг/м 2 ежедневно, парентерально.
Нередко для постоянной заместительной терапии необходимо сочетанное введение и минералокортикоидов. Для этого используют препарат минералокортикоидов для перорального применения, 9α-флудрокортизон (Кортинеф, Флоринеф) в дозе 0.5-1 мг/сутки в большинстве случаев. При необходимости, например в случае тяжёлой, сольтеряющей формы ВДКН, эту дозу увеличивают. При этом даже при простой, вирильной или компенсированной (без потери солей) форме ВДКН введение небольших количеств препарата может улучшить эффективность компенсации.
Ятрогенная надпочечниковая недостаточность.
В последние десятилетия применение глюкокортикоидов при лечении самых различных болезней и патологических состояний в периоде новорождённости вошло в широкую медицинскую практику. К сожалению, именно у новорождённых описано немало случаев развития надпочечниковой недостаточности из-за применения слишком больших доз глюкокортикоидов или их слишком длительного применения. Использование больших доз глюкокортикоидов, но непродолжительное время (менее 7 дней) не опасно, но при длительном их применении (более 30 дней) развивается как минимум транзиторная надпочечниковая недостаточность. Большое значение имеет и режим отмены препарата, т.к. при быстрой их отмене можно ухудшить состояние ребёнка.
После длительной глюкокортикоидной терапии дозу препаратов необходимо снижать постепенно на 50% каждые несколько дней, пока не будет достигнута поддерживающая доза (по гидрокортизону – 10 мг/м 2 в сутки per os). После этого дальнейшее снижение проводят более осторожно, по 20% каждые 4-5 дней. При этом даже при отсутствии тех или иных клинических признаков надпочечниковой недостаточности после отмены препаратов ещё какое-то время, по-видимому, надпочечники остаются в состоянии подавления и не всегда смогут отреагировать адекватно на стрессовую ситуацию. Целенаправленных исследований по изучению корреляции дозы и продолжительности глюкокортикоидной терапии со временем, необходимым для полного восстановления функции надпочечников после прекращения не проводилось, но описаны случаи развития надпочечниковой недостаточности на фоне стрессовой ситуации через 6 месяцев и более после их отмены. По-видимому, после длительной, с высокими дозами глюкокортикоидной терапии в течение как минимум 1 года на время возникновения стрессовой ситуации показано профилактическое назначение гидрокортизона в дозе 30 мг/м 2 /сутки, перорально.
Надпочечниковая недостаточность: симптомы и лечение у женщин, мужчин и детей
Поскольку часть кортикостероидов все же продуцируется, симптоматика недостаточности надпочечников появляется лишь в случае, требующем повышенной секреторной активности органов.
Первичная форма надпочечниковой недостаточности развивается в результате дисфункции самих надпочечников. Аномалия может возникнуть на фоне генетических отклонений или аутоиммунных процессов.
Существуют и другие факторы, провоцирующие дефицит кортикостероидов:
- туберкулез;
- острая кровопотеря;
- онкология с метастазами в надпочечник;
- амилоидоз;
- обширная интоксикация организма;
- тяжелое инфекционное заболевание (сепсис, менингококковая инфекция, скарлатина, грипп, дифтерия);
- тромбоз вен надпочечников;
- тройной синдром;
- синдром Кернса-Сейра;
- некроз тканей органа.
Вторичная надпочечниковая недостаточность формируется при различных поражениях гипофиза. Это могут быть опухоли, кровоизлияния после травм, операции, продолжительный прием глюкокортикоидов.
Гипокортицизм в детском возрасте обычно носит первичный характер, обусловленный наследственными патологиями. Риск возникновения недостаточности надпочечников существенно увеличивается при любом поражении эндокринной системы, в случае проведения лучевой терапии или операции на гипофизе и гипоталамусе.
Острая надпочечниковая недостаточность у детей развивается под воздействием инфекций, спровоцированных стафилококком, аутоиммунных заболеваний, сильного стресса, кровоизлияния в орган.
Классификация
Существует несколько систематических групп гипокортицизма. Так, по причинному фактору определяется:
- первичная надпочечниковая недостаточность или болезнь Аддисона. Развивается при разрушении 95% корковых тканей. Встречается довольно редко;
- вторичная надпочечниковая недостаточность, обусловленная поражением гипофиза, приводит к дефициту кортикостероидов (АКГТ), активирующих работу надпочечников.
Существует еще третичный гипокортицизм, развивающийся при заболеваниях гипоталамуса и ятрогенное расстройство, вызываемое отменой глюкокортикоидов после их продолжительного приема.
Вторичная и третичная недостаточность коры надпочечников объединяются термином — центральный гипокортицизм.
По типу протекания существует:
- Острая недостаточность коры надпочечников. Наступает, если корковое вещество резко снижает или вовсе прекращает синтез гормонов. Развивается стремительно.
- Хроническая надпочечниковая недостаточность (ХНН).Протекает медленно, с мало выраженными симптомами, поэтому диагностируется не сразу. Терапии поддается плохо и приводит к большому числу осложнений.
Острая форма гипокортицизма требует срочной госпитализации.
Заболевание прогрессирует очень медленно. Первые симптомы надпочечниковой недостаточности проявляются, когда орган практически полностью разрушен. Толчком к их появлению становится стресс, перенесенная инфекция, травма, сильная кровопотеря.
Основные признаки хронического гипокортицизма:
- астения;
- гиперпигментации кожи и слизистых;
- расстройства пищеварения, ухудшение аппетита, рвота;
- потеря массы тела;
- гипотензия;
- повышенная утомляемость, снижение работоспособности.
Иногда у больных отмечается полная потеря интереса к жизни, семье и детям.
Острая надпочечниковая недостаточность (адреналовый криз) протекает значительно интенсивнее. Патологическое состояние может быть представлено следующими клиническими формами:
- Сердечно-сосудистой. Проявляется нарушением кровотока: бледностью, тахикардией, гипотонией, похолоданием конечностей, прекращением выделения мочи, коллапсом.
- Желудочно-кишечной. Напоминает пищевое отравление с резкими болями в животе, диареей, метеоризмом, рвотой.
- Нервно-психической. Выражается судорогами, заторможенностью сознания, бредом, галлюцинациями, мигренями.
Если аддисонический криз не купировать вовремя, он может привести ко множественным осложнениям и гибели пациента.
Симптоматика поражения надпочечников у мужчин имеет свои особенности. У всех представителей сильного пола постепенно меняется внешний вид, развивается гинекомастия. В районе живота, груди и плеч появляются избыточные жировые отложения, лицо приобретает луноподобную форму. На передней брюшной стенке и бедрах возникают растяжки.
Еще один типичный симптом хронической надпочечниковой недостаточности у мужчин — потеря сексуального желания и ухудшение потенции.
Неспособность забеременеть и выносить ребенка — частая проблема, с которой сталкиваются дамы, страдающие недостаточностью надпочечников. Сниженное продуцирование гормонов вызывает у женщин множество изменений в работе организма.
Патология проявляется следующими характерными симптомами:
- уменьшением размера молочных желез и матки;
- увеличением клитора;
- нарушением месячного цикла;
- бесплодием;
- обильной угревой сыпью на лице и теле.
Если беременность все же наступает, то протекает тяжело и нередко заканчивается выкидышем. В случае родов малышу может грозить наследственная патология.
У девушек, как и у женщин, при недостаточности надпочечников наблюдается аменорея или задержка менструаций. Девочки часто отстают от сверстниц в половом развитии, отличаются худобой и узким тазом.
Какой врач лечит надпочечниковую недостаточность?
При появлении симптомов заболевания необходимо подойти к эндокринологу. В его отсутствие медицинскую помощь может оказать терапевт или врач общей практики.
Диагностика
Диагностика надпочечниковой недостаточности базируется на проведении лабораторных исследований. Анализы показывают, каких именно гормонов не хватает и насколько выражен дефицит.
Скрытые формы патологии выявляет стимуляционная проба с АКТГ. Тест выполняют утром, когда отмечается естественный пик изучаемых гормонов.
Для определения типа поражения проводят ряд инструментальных обследований:
- УЗИ.
- МРТ надпочечников и головного мозга.
- ЭКГ.
Поставить более точный диагноз помогает серологический скрининг. Эту методику обычно используют для выявления атрофии тканей надпочечника.
Лечение надпочечниковой недостаточности направлено на замещение нехватки гормонов и ликвидацию причин, вызвавших патологическое состояние. Огромные разрушения коркового вещества необратимы, поэтому пациент нуждается в пожизненном применении гормонов.
Терапия у женщин и мужчин проводится одинаковыми препаратами. Чаще всего больным с надпочечниковой недостаточностью назначают:
- Кортизол (Гидрокортизон). Глюкокортикоид идентичен натуральному гормону.
- Кортизон. Претерпевает изменения в печени и превращается в кортизол.
- Преднизолон. Назначают чаще всего.
- Метилпреднизолон. Имеет меньше противопоказаний, чем Преднизолон.
- Триамцинолон (Леналог). Может спровоцировать миопатию.
- Дексаметазон (Фортекортин). Сильный ингибитор АКТГ.
- Кортинеф (Флоринеф).
Распространенной ошибкой при заместительном лечении первичных нарушений является применение только глюкокортикоидов.
Критерием успешности гормональной терапии считается восстановление массы тела, исчезновение гиперпигментации и гипогликемии, улучшение самочувствия.
Осложнения
Наиболее серьезным осложнением гипокортицизма принято считать надпочечниковый криз, который нередко приводит к коматозному состоянию. При этом отмечается нарастание паники, падение АД, неукротимая рвота с последующим обезвоживанием организма, нарушение сердечного ритма.
Профилактика
Специфической профилактики надпочечниковой недостаточности не существует. Основным способом предупреждения болезни является недопущение воздействия на организм внешних и внутренних негативных факторов.
Лицам, имеющим врожденную предрасположенность к гипокортицизму или длительное время принимающим препараты кортикостероидов, рекомендуется периодически проходить медико-генетическую экспертизу.
Для профилактики врожденного поражения надпочечников беременной женщине необходимо оградить себя от воздействия отравляющих веществ, наркотиков, алкоголя.
Инвалидность
Больным, страдающим гипокортицизмом, не рекомендуется тяжелый физический и умственный труд, нервное перенапряжение, наличие производственных вредностей. В противном случае возникает заметное ухудшение состояния с переходом в острую форму.
На этом основании пациентам присваивается группа инвалидности, зависящая от тяжести заболевания:
- I группа — показана больным с хронической недостаточностью надпочечников, сопровождающейся поражением сердечной мышцы и аддисоническими кризами.
- II группа — назначается людям с ограничениями к передвижениям и тяжелому труду, способным выполнять несложную работу в комфортных условиях.
- III группа — присваивается лицам с легкой степенью поражения надпочечников, ограничивающей производственную деятельность в тяжелых и вредных условиях.
При назначении группы инвалидности пациентам со вторичной ХНН необходимо учитывать тяжесть поражения ЦНС и внутренних органов.
Надпочечниковая недостаточность является сложным и опасным заболеванием, которое крайне негативно отражается на работе всего организма. При появлении подозрительной симптоматики следует сразу обратиться к специалисту. К сожалению, полностью победить болезнь невозможно, поэтому пациенту придется всю оставшуюся жизнь принимать гормональные лекарства.
Вторичная надпочечниковая недостаточность
Причина вторичной надпочечниковой недостаточности — дефицит АКТГ, который может быть изолированным (например, при длительной глюкокортикоидной терапии) или сопровождаться дефицитом других гормонов гипофиза («Гипогапуитаризм»).
Клиническая картина при вторичной надпочечниковой недостаточности почти такая же, как при первичной; единственное отличие состоит в том, что у большинства больных не развивается гиперпигментация, поскольку уровень АКТГ и других производных проопиомеланокортина (в частности, МСГ) в крови снижен. Уровень АКТГ в плазме — это основной критерий, позволяющий различить первичную и вторичную надпочечниковую недостаточность: в первом случае уровень АКТГ повышен, а во втором — снижен или АКТГ не определяется.
При гипопитуитаризме наблюдаются признаки дефицита многих гормонов. Вторичная надпочечниковая недостаточность не сопровождается гипоальдостеронизмом.
При гипопитуитаризме иногда отмечается гипонатриемия, которая возникает либо в результате увеличения ОЦК, либо из-за недостаточного усиления секреции альдостерона при ограничении потребления поваренной соли. Вместе с тем, сильное обезвоживание, гипонатриемия и гиперкалиемия указывают на тяжелый дефицит минералокортикоидов и говорят в пользу первичной надпочечниковой недостаточности.
Длительный прием глюкокортикоидов приводит не только к экзогенному синдрому Кушинга, но и к надпочечниковой недостаточности в результате продолжительного угнетения гипотадамо-гипофизарной системы и атрофии надпочечников, не стимулируемых АКТГ. Помимо снижения секреции АКТГ гипофизом, у больных отмечается резистентность надпочечников к действию этого гормона. Характерны снижение уровня кортизола и АКТГ и экскреции стероидов с мочой, а также отсутствие реакции на пробы с АКТГ и метирапоном.
У большинства больных функция гипоталамо-гипофизарно-надпочечниковой системы восстанавливается после отмены глюкокортикоидов, но на это может потребоваться разное время — от нескольких дней до нескольких месяцев. Самый быстрый способ проверить, восстановилась ли функция этой системы, — короткая проба с АКТГ.
При ее проведении уровень кортизола в плазме изменяется так же, как и после гипогликемической пробы с инсулином, и по этим изменениям можно судить о состоянии гипоталамо-гипофизарно-надпочечниковой системы (см. выше, «Оценка функции гипофизарно-надпочечниковой системы»). Кроме того, можно определить резерв АКТГ с помощью проб с метирапоном и инсулином.
Вторичную надпочечниковую недостаточность лечат глюкокортикоидами точно так же, как и первичную. В назначении минералокортикоидов нет необходимости, поскольку секреция альдостерона не нарушена.
Острая надпочечниковая недостаточность
Причины острой надпочечниковой недостаточности разнообразны. Так, сопутствующие заболевания, особенно сепсис, или хирургическое вмешательство у больных с хронической надпочечниковой недостаточностью могут привести к гипоадреналовому кризу. Другой его причиной может быть двустороннее кровоизлияние в надпочечники.
У детей оно может быть спровоцировано псевдомонадным или менингококковым сепсисом (синдром Уотерхауса—Фридериксена), а у взрослых — лечением антикоагулянтами или нарушением свертывания крови.
Изредка двустороннее кровоизлияние в надпочечники возникает при родовой травме. Инфаркт надпочечников может быть следствием тромбоза надпочечниковой вены, например при антифосфолипидном синдроме (особенно во время беременности), или осложнением флебографии надпочечников (например, кровоизлияние в аденому).
Третья и наиболее частая причина острой надпочечниковой недостаточности — это резкая отмена глюкокортикоидов после их длительного приема. Острая надпочечниковая недостаточность может возникать также у больных с врожденной гиперплазией коры надпочечников или пониженным резервом глюкокортикоидов при назначении препаратов, подавляющих синтез стероидов (митотан, кетоконазол) или ускоряющих их метаболизм (фенитоин, рифампицин).
Гипоадреналовый криз
Продолжительность жизни больных с надпочечниковой недостаточностью во многом зависит от
успеха профилактики и лечения гипоадреналовых кризов. При инфекциях, травмах, хирургических вмешательствах, желудочно-кишечных нарушениях и других сопутствующих заболеваниях следует немедленно увеличить дозу глюкокортикоидов. У нелеченных больных проявления надпочечниковой недостаточности прогрессируют.
Наблюдаются стойкие тошнота, рвота и боль в животе. Лихорадка может быть высокой или, наоборот, отсутствовать. Нарастает угнетение сознания, а обезвоживание вызывает падение АД, которое быстро приводит к обмороку. У больных, получающих заместительную терапию, обычно не бывает дефицита минералокортикоидов, поэтому обезвоживание и артериальная гипотония нередко возникают лишь в терминальной стадии. При гипоадреналовом кризе всегда следует выяснить его причину.
Диагностическая тактика при подозрении на надпочечниковую недостаточность
При вторичной надпочечниковой недостаточности уровень АКТГ в плазме низкий. При надпочечниковой недостаточности, обусловленной опухолями гипофиза, и при идиопатическом гипопитуитаризме отмечается дефицит других гормонов гипофиза. С другой стороны, возможен и изолированный дефицит АКТГ, например при длительном приеме глюкокортикоидов.
Однократное измерение уровня гормонов малоинформагивно. поэтому для подтверждения диагноза нередко проводят пробу с инфузией тетракозактида в течение 24 ч. Отличить больных вторичной надпочечниковой недостаточностью от здоровых людей можно с помощью проб с инсулином или метирапоном.
Основная цель лечения — восполнить дефицит глюкокортикоидов, натрия и воды. Начинают инфузию 5% глюкозы в физиологическом растворе и струйно вводят 100 мг гидрокортизона, а затем переходят на длительную инфузию гидрокортизона со скоростью 10 мг/ч. При другом варианте лечения вводят по 100 мг гидрокортизона в/в струйно каждые 6 ч.
Однако поддерживать концентрацию кортизола в плазме на уровне, необходимом при стрессе (более 830 нмоль/л, или 30 мкг%), удается лишь с помощью длительной инфузии гидрокортизона. Заместительная терапия глюкокортикоидами и восполнение дефицита натрия и воды способствуют устранению артериальной гипотонии. Если гипоадреналовому кризу предшествовали тошнота, рвота и обезвоживание, в первые часы необходимо ввести несколько литров физиологического раствора.
При тяжелом состоянии помимо восполнения объема могут потребоваться сосудосуживающие средства (например, дофамин). Поскольку в большой дозе (100—200 мг) гидрокортизон обладает минералокортикоидной активностью, дополнительного назначения минералокортикоидов не требуется. При улучшении состояния дозу гидрокортизона в течение нескольких дней понижают до поддерживающей и при необходимости снова назначают минералокортикоиды.