Гиэ это что
Перинатальная гипоксически-ишемическая энцефалопатия новорожденных: новый метод лечения
Что такое перинатальная гипоксически-ишемическая энцефалопатия?
Перинатальная гипоксически-ишемическая энцефалопатия (ГИЭ) – это следствие недостаточного кровоснабжения головного мозга ребенка во время беременности матери, родов или в течение первого месяца его жизни. Гипоксия-ишемия головного мозга является основной причиной неврологических повреждений у новорожденных. Одними из основных параметров, характеризующих тяжесть гипоксически-ишемического поражения головного мозга в родах и во время беременности, являются оценка по шкале Апгар и наличие мекония в околоплодных водах.
Последствия ГИЭ могут быть различными: от незначительного снижения внимания и неусидчивости ребенка до тяжелых форм детского церебрального паралича.
Дети с умеренной степенью поражения мозга могут выглядеть здоровыми в течение первых дней и даже месяцев жизни. Патология у них выявляется при проведении УЗИ головного мозга на первом месяце жизни, при осмотре неврологом и другими специалистами.
Детям с тяжелой формой ГИЭ и асфиксией в родах, как правило, требуется интенсивная терапия, и они проходят поэтапное лечение в родильном доме и отделении патологии новорожденных.
Перинатальная гипоксически-ишемическая энцефалопатия умеренной и тяжелой степени является одним из основных факторов риска развития ДЦП.
Течение ГИЭ очень индивидуально, но, как правило, оно сопровождается гибелью части клеток головного мозга и требует своевременного и правильного лечения. Соблюдение этого принципа позволяет добиться существенного улучшения даже при тяжелом поражении головного мозга.
Какое лечение назначают при ГИЭ?
Лучшим лечением ГИЭ являются профилактика и ранняя терапия внутриутробной гипоксии и асфиксии новорожденного. Но, несмотря на значительные успехи в профилактике осложнений родов, умеренная и тяжелая гипоксически-ишемическая энцефалопатия по-прежнему встречается с частотой 1–2 на 1000 родившихся детей. До недавнего времени медицина могла предложить таким детям лишь поддерживающую терапию дисфункции органов.
С 2010 года стандартом лечения ГИЭ стала индуцированная гипотермия. Этот метод заключается в том, что начиная с 6 часов после рождения температуру тела ребенка в течение 72 часов поддерживают на уровне 33,5 °С. К сожалению, даже после применения индуцированной гипотермии у значительного числа младенцев с ГИЭ сохраняются неврологические расстройства различной степени тяжести.
Сегодня для лечения новорожденных с ГИЭ ученые предлагают новый метод – регенеративную терапию стволовыми клетками пуповинной крови.
Новый метод лечения ГИЭ
При ГИЭ используют мононуклеарную фракцию пуповинной крови, содержащую стволовые клетки. Когда ее вводят ребенку внутривенно, происходят восстановление и регенерация клеток головного мозга, регулируется работа иммунной системы. Если терапию начали проводить на раннем этапе заболевания, то энцефалопатия может быть излечена за счет мощного регенеративного потенциала пуповинной крови и восстановления популяции нервных клеток. Уникальность клеточной терапии при энцефалопатии заключается в достижении высоких результатов лечения в каждом случае. На сегодня только в России уже спасено более 330 детей, страдающих ДЦП, с помощью заготовленной пуповинной крови.
Лечение гипоксически-ишемической энцефалопатии мононуклеарной фракцией пуповинной крови на ранних этапах является важнейшим фактором благоприятного прогноза, снижения риска развития ДЦП, а также правильного развития ребенка и улучшения качества его жизни в последующие годы.
Таким образом, приняв решение о сохранении пуповинной крови, родители дают своему малышу замечательную «биологическую страховку» от ДЦП: при необходимости к лечению можно приступить с первого дня жизни новорожденного, используя его же собственные клетки пуповинной крови, прямо в родильном доме.
Родители – будьте бдительны: заготовьте пуповинную кровь своего ребенка и тем самым вы спасете его от многих заболеваний.
Гиэ это что
Гипоксически-ишемическая энцефалопатия (ГИЭ) встречается примерно у 1-6 из 1000 живорожденных и является самой важной проблемой неонатальной неврологии (Levene et al., 1985, Volpe, 2001, Ferriero, 2004). Гипоксически-ишемическая энцефалопатия (ГИЭ) относится к серьезным состояниям, при котором 15-20% пострадавших детей умирает в течение неонатального периода, а у 25% развиваются стойкие неврологические последствия (Volpe, 2008). Более двадцати лет назад было отмечено завышенное значение перинатальной гипоксии в этиологии задержки умственного развития и церебрального паралича (Freeman и Nelson, 1988, Вах и Nelson, 1993).
Badawi et al. (1998) обнаружили, что многие новорожденные подвергались антенатальным факторам риска, таким как лечение материнского бесплодия или заболеваний щитовидной железы, тогда как другие имели и анте-, и интранатальные факторы риска. Хотя не исключается возможность наличия пренатальных факторов риска, вероятно повышающих чувствительность ребенка к проблемам родового периода, в проспективном исследовании результатов MPT Cowan et al. (2003) было отмечено, что у большинства новорожденных (n=351) с неонатальной энцефалопатией повреждение мозга возникало в момент рождения или незадолго до этого.
Определение гипоксически-ишемической энцефалопатии (ГИЭ) сложное и роль асфиксии в родах трудно точно установить, так что и сам термин ставится под сомнение; вместо него предлагается неопределенное понятие «неонатальная энцефалопатия» (Nelson и Leviton, 1991, Leviton и Nelson, 1992, Badawi et al, 1998). Диагноз ГИЭ не должен устанавливаться без серьезной клинической основы и тщательного анализа альтернативных вариантов, потому что они могут играть роль в терапии и этиологии.
Патофизиология. Недостаточное поступление кислорода, вызывающее развитие гипоксической-ишемической энцефалопатии (ГИЭ), может возникнуть по двум механизмам: гипоксемия, т.е. ограниченный доступ кислорода в кровь; и ишемия, т.е. сниженная перфузия головного мозга. В большинстве случаев оба механизма связаны с асфиксией в виде гипоксии, сопровождающейся гиперкарбией (Altman et al., 1993). Обычно присутствующий при гипоксии ацидоз в значительной степени связан с повышенным образованием лактата. Преобразование глюкозы в молочную кислоту менее эффективно, чем окисление в цикле Кребса и митохондриальной системе транспорта электронов.
В результате окисления каждой молекулы глюкозы, переработанной в анаэробных условиях, образуется только две молекулы аденозина дифосфата (АДФ) по сравнению с 38 молекулами при аэробных условиях. Несмотря на значительное повышение скорости гликолиза и усиление мозгового кровотока из-за ацидоза и гиперкапнии (Laptook et al., 1988), потребности ткани мозга в кислороде не могут быть удовлетворены. Повышенная скорость гликолиза приводит к падению уровня глюкозы в мозге. Предупреждение этого состояния предварительным введением глюкозы повышает выработку АТФ и улучшает выживаемость (Vannucci и Yager, 1992). Однако избыточный уровень глюкозы в то же время приводит к повышенному образованию лактата, вредного для мозговой ткани взрослого, но, по-видимому, полезного для ЦНС новорожденного (Hattori и Wasterlain, 1990).
В итоге, в результате нехватки кислорода в клетках мозга снижается количество фосфокреатина и АТФ, конечных акцепторов электронов. Эти изменения были продемонстрированы у новорожденных с использованием фосфорной МРС (магнитно-резонансная спектроскопия) (Younkin et al., 1988, Laptook et al., 1989). Падение уровня высокоэнергетических соединений фосфата наблюдалось даже при стабилизации кардиопульмональной функции (Hope et al., 1984). В экспериментах на животных снижение уровня АТФ более чем на 30% происходило за 6 минут (Raichle, 1983). Также было отмечено накопление лактата, сохранявшееся в течение длительного периода времени (Groenendaal et al, 1994, Robertson et al., 1999).
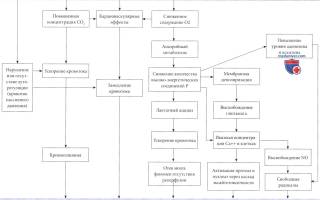
Механизм повреждения мозга при гипоксически-ишемической энцефалопатии.
Нейрональные повреждения являются следствием различных комбинаций кровоизлияний и некрозов.
Последние связаны с каскадом событий, инициированных высвобождением глютамата, приводящим к массивному входу кальция в клетки.
Образование оксида азота (NO), вероятно, также является важным фактором.
В действительности, нарушению мозговой функции предшествует сбой в энергетическом метаболизме (см. Volpe, 2001). При угрозе перебоев организм отвечает угнетением нейрональной активности по неопределенному механизму, но при длительной гипоксии этого недостаточно.
Однако мозг новорожденного чрезвычайно устойчив к гипоксии. При экспериментах на плодах обезьян потребовалось снижение сатурации кислорода на 90% в течение не менее 25 минут, чтобы вызвать повреждение ткани мозга. В результате, любой, достаточно тяжелый для повреждения мозга эпизод асфиксии вызывает нарушения и других органов, особенно сердца, и при таких условиях ишемия постоянна.
Ишемия оказывает влияние, подобное асфиксии (Painter, 1989). Процесс гликолиза ускоряется, но поглощению глюкозы препятствует нарушение кровотока, соответственно запасы высокоэнергетических фосфатов истощаются, и накапливается лактат.
Влияние гиперлактатемии многопланово. Первоначально оно благотворно, поскольку повышает приток крови к мозгу, но затем становится вредным, так как хотя бы отчасти влияет на отек мозга, который в свою очередь может сдавить капиллярное русло и вызвать ишемию (Myers, 1972). В то же время он нарушает ауторегуляцию церебрального кровообращения, приводя к мозговому кровотоку пассивного давления (Lou, 1988), что делает мозг более чувствительным к изменениям системного давления крови. Сочетание отека мозга и системной недостаточности кровообращения, вероятно, играет существенную роль в происхождении гипоксического повреждения ЦНС. Гипоксия обычно повышает долю сердечного выброса, предназначенную для головного мозга.
По мере усиления степени гипоксии наблюдается уменьшение сердечного выброса с последующей неспособностью поддерживать артериальное давление на необходимом уровне. Но показатели частоты сердечных сокращений и артериального давления остаются неизменными до тех пор, пока артериальная сатурация не снизится более, чем на 65%, а затем также линейно снижаются. Это снижение может поддерживаться на протяжении часов без развития энцефалопатии, если содержание кислорода в артериальной крови не упадет более, чем на 85% (Fenichel, 1997).
Механизм отека мозга и гипоксического повреждения у плодов до конца неясен. Levene et al. (1989) выявили хорошую корреляцию между высокой скоростью мозгового кровотока—предположительно отражающей церебральную гиперемию, которая, в свою очередь, может отвечать за повышение внутричерепного давления — и неблагоприятным течением. Lupton et al. (1988) показали, что отек в большей степени является следствием, чем причиной, нейрональных некрозов, объясняя, таким образом, ограниченную эффективность противоотечного лечения новорожденных с ГИЭ (Levene et al., 1987). Не было замечено различий в степени внутричерепной гипертензии у детей с ГИЭ в группе выживших и умерших (Goitein et al, 1983).
Последние данные подтверждают основную роль апоптоза в развитии гипоксически-ишемического повреждения мозга новорожденных, возможно, даже большую, чем некроз после повреждения. Во время неонатального поражения мозга токсичность возбуждающих медиаторов, оксидативный стресс и воспаление способствуют ускоренной гибели клеток, главным образом, посредством апоптоза или некроза, что зависит от области поражения и тяжести повреждения. В настоящее время известно, что ГИЭ состоит из двух последовательных стадий, с окончательным повреждением с отсрочкой на несколько часов во время второй из них, определяемой как вторичная недостаточность энергии. Тем не менее, профилактика возможна, как только появляется терапевтическое окно.
Механизмы повреждения и некроза клеток при гипоксии и ишемии не просто итог энергетической недостаточности. Это вторичные пусковые факторы каскада разрушительных событий при достижении критического уровня дефицита энергии. Такие события происходят в течение нескольких часов. Избыточная мембранная деполяризация и высвобождение возбуждающих аминокислотных нейротрансмиттеров, в первую очередь глютамата (Lipton и Rosenberg, 1994), приводит к массивному входу кальция через NMDA и АМРА мембранные рецепторы (Morley et al., 1994) и к накоплению кальция в цитозоле. Кальций, в свою очередь, активирует различные липазы, протеазы и нуклеазы с последующим разрушением основных клеточных белков. Свободные радикалы прямо или косвенно вызваны повышенным уровнем кальция в цитозоле (McCord, 1985) и оксида азота (Dawson et al., 1992), играющего главную роль в их образовании.
Этот каскад возбуждающих медиаторов в конечном счете приводит к повреждению мембраны, разрушению цитоскелета и, наконец, к дезинтеграции клетки.
Теоретически существует возможность предотвращения многих процессов, поэтому проводились исследования с различными средствами, в том числе блокаторами кальциевых каналов (Miller, 1993, Palmer и Vanucci, 1993); антагонистами возбуждающих аминокислот (Hattori et al., 1989), особенно магнезией (Marret et al., 1995, Nelson и Grether, 1995); ингибиторами синтеза оксида азота (Dawson et al., 1992); акцепторами свободных радикалов (Palmer и Vannucci, 1993) и веществами, подавляющими образование свободных радикалов типа аллопуринола (Palmer et al., 1990, van Bel et al., 1998, Benders et al., 2006).
Редактор: Искандер Милевски. Дата публикации: 25.11.2018
Гипоксически ишемическое поражение головного мозга
Нехватка кислорода в организме человека в считаные секунды наносит иногда непоправимый вред. Гипоксически-ишемическая энцефалопатия (ГИЭ) иногда звучит страшным приговором как для ребенка, так и для взрослого. Давайте разберемся, что это за болезнь, ее симптомы и насколько опасно гипоксически-ишемическое поражение головного мозга в любом возрасте.
Особенности патологии
Дефицит кислорода неизбежно отражается на функционировании организма. Гипоксически-ишемическая энцефалопатия у новорожденных случается часто: как у доношенных деток, так и недоношенных. У 10% младенцев, перенесших ее, в дальнейшем ставят диагноз «ДЦП». Именно поэтому будущая мать должна чаще бывать на свежем воздухе и точно соблюдать рекомендации врача, чтобы снизить риск гипоксии до минимума.
У взрослых частой причиной патологии становятся травмы или имеющиеся серьезные заболевания. Если при приступе удушья помощь не будет оказана вовремя, то есть серьезный риск летального исхода или инвалидности. Немаловажную роль играет и степень тяжести патологии, чем она выше, тем меньше шансов у человека на возврат к полноценной жизни.
Когда наступает кислородное голодание в важнейшей части центральной нервной системы, это приводит к дефициту этого вещества в клетках мозга, что замедляет кровоток и все метаболические процессы. При таком недостатке питания нейроны мозга в некоторых участках органа начинают отмирать, приводя к неврологическим нарушениям.
Ускоряет процесс отек мозга, возникающий также из-за сбоя в кровообращении. Давление растет, и клетки начинают быстрее гибнуть. Чем быстрее проходит процесс, тем больше шансов на то, что повреждения будут необратимыми.
Причины возникновения
Гипоксическая энцефалопатия у взрослых и у детей возникает по разным причинам. Их важно знать, чтобы принять все меры для ее предупреждения.
У взрослых
Гипоксическая ишемическая энцефалопатия возникает на фоне нехватки кислорода, к чему приводят следующие причины:
- состояние удушья;
- удушение;
- сбой дыхательной системы любого рода происхождения;
- наркотическая зависимость, передозировка;
- патологии кровеносной системы, приводящие к ее непроходимости или разрыву;
- цианид, окись углерода — отравление;
- длительное пребывание в задымленном месте;
- травма трахеи;
- остановка сердца;
- болезни, приводящие к параличу мышечной ткани дыхательной системы.
Острая гипоксическая энцефалопатия наступает, если кислород не поступал в организм несколько минут. Это тяжелое течение патологии, которое чаще всего заканчивается летальным исходом. Зафиксированы единичные случаи, когда люди выживали, но для них это заканчивалось тяжелой формой серьезных психических болезней.
У новорожденных
Причиной такого состояния у только родившегося ребенка может быть:
- удушье во время родов из-за слабой родовой деятельности;
- преждевременный родовой процесс или с патологическими факторами, такими как выпадение пуповины;
- болезни инфекционного генеза у матери;
- ряд физических факторов от грязного воздуха до радиационного излучения.
Именно асфиксия у грудничков является самым частым фактором, приводящим к ГИЭ. Врачи выделяют следующие факторы риска для ее возникновения:
- гипотония острой формы у роженицы;
- недоразвитость легких, что приводит к недостатку кислорода в крови;
- сложности в работе сердца;
- травмирование плода узким тазом матери или из-за проблем с пуповиной;
- сложности в родовой деятельности, травма, стресс;
- гипоксия;
- родовое кровотечение;
- халатность медицинского персонала;
- отслойка плаценты;
- изменение формы черепа плода из-за давления;
- родовая травма, разрыв матки;
- низкое предлежание плаценты.
Степени тяжести и характерные симптомы
Гипоксически-ишемическая энцефалопатия имеет 3 степени тяжести, для которых характерны свои проявления. По ним врачи часто дают предварительную характеристику повреждений мозговой деятельности и приблизительный прогноз.
Легкая степень
При такой степени у больного будет:
- расширен зрачок и широко открыты веки;
- отсутствовать концентрация внимания;
- нарушена координация движений, блуждающее поведение;
- выявлена либо сонливость, либо гипервозбудимость;
- высокая степень раздражительности;
- отсутствовать аппетит;
- нарушено мозговое кровообращение.
Средняя степень
Неврология при ней будет более выражена, т. к. нарушение насыщения мозга кислородом более длительное:
- у малыша спонтанные крики без причины;
- защитный и опорный рефлекс либо ослаблен, либо отсутствует вовсе;
- признаки мышечной слабости;
- опущение верхнего века;
- увеличение давления цереброспинальной жидкости;
- метаболический ацидоз крови;
- невралгические приступы;
- сбой в глотательном процессе.
Тяжелая степень
Поражение в таких случаях более тяжелое, что проявляется в:
- судорожности;
- синюшности кожи;
- потере сознания;
- гипертензии;
- отсутствии двигательных возможностей;
- косоглазии;
- коме или прекоме;
- отсутствии реакции зрачков на свет;
- сбое дыхательного процесса с сильной аритмией;
- тахикардии.
ПЭП — это разновидность гипоксически-ишемической энцефалопатии у детей раннего возраста. Ее диагностируют как сразу после рождения, так и на первом году жизни. Развивается ПЭП как внутриутробно, в процессе родовой деятельности, так и в первые 10 дней с момента рождения.
Она может быть трех степеней тяжести с характерной симптоматикой и протекать в острой форме — до месяца, в раннем восстановлении функций — до 4 месяцев, при позднем восстановлении — до 2 лет.
Диагностика
Перинатальный синдром ишемии на фоне гипоксии мозга начинают диагностировать, делая визуальный осмотр ребенка. Так же и со взрослыми. Несмотря на все достижения медицины, уникальный тест, позволяющий точно выявить ГИЭ, до сих пор не придуман. Все лабораторные методики направлены на выявление того, насколько сильно поврежден мозг и текущее состояние всего организма.
Какими будут исследования, зависит от симптомов, и как они развивались. Для расшифровки анализов есть специальные биомаркеры, которые дают полную картину о степени ГИЭ. Для исследования нужна кровь больного.
Нейровизуализацию проводят с помощью:
- нейросонографа и/или МРТ, томографа, показывающего внутренние повреждения мозга и изменения в нем;
- доплерографа, фиксирующего работу мозгового кровотока;
- электронейромиографа для определения чувствительности волокон периферии нервной системы.
Дополнительного могут использовать:
- электроэнцефалограф для выявления задержки развития на ранней стадии и есть ли эпилепсия;
- видеомониторинг для изучения двигательной активности малышей.
При необходимости пострадавшего осматривает окулист, чтобы определить состояние зрительных нервов и глазного дна, а также на наличие болезней генетического типа в этой области.
Лечение и уход
За пострадавшими должен быть особый уход, а за детьми, перенёсшими ГИЭ, он строится на контроле за:
- температурой в помещении — не более 25 градусов;
- его комфортной позой, поэтому тугое пеленание под запретом;
- тем, чтобы свет был мягким и приглушенным;
- тишиной;
- кормлением, которое должно быть с контактом «кожа к коже» и согласно потребностям малыша;
- дыханием, при сбое в котором подключают специальный аппарат.
- Хирургически, для восстановления и улучшения кровообращения в мозгу. Чаще всего для этих целей используют эндоваскулярную методику, которая не нарушает целостность тканей.
- Медикаментозно, выбирая препараты в зависимости от того, насколько тяжелая степень поражения и ее клинической картины.
- На антиконвульсантах, которые купируют судороги. Обычно это Фенобарбитал, дозировку которого подбирают индивидуально. Внутривенный способ самый быстрый. Но сам препарат противопоказан при сверхчувствительности, тяжелой форме гипоксической и гиперкаптической дыхательной недостаточности, проблемах с почкам и печенью, при беременности. Может быть использован Лоразепам, у него аналогичное воздействие и список противопоказаний.
- На сердечно-сосудистых средствах, чтобы увеличить системное сопротивление сосудов и сократительную функцию миокарда, что приводит к повышенному сердечному выбросу. Все средства этой группы влияют на почки, а при передозировке побочные эффекты предсказать сложно. Чаще всего используют Допамин, Добутамин.
Дальнейшее наблюдение
Из стационара выписывают только после прохождения полного курса физической терапии и комплексной оценки нервно-психического развития. Чаще всего после выписки пациенты не требуют специфического ухода, но регулярные осмотры в клинике обязательны, особенно для детей.
Если болезнь была тяжелой, то ребенок будет наблюдаться в специальном центре, где ему будет помогать врач по нервно-психическому развитию.
Лечение судорожности зависит от симптоматики центральной нервной системы и результатов исследований. Выписывают только с легким отклонением от нормы или вовсе в ее пределах. Фенобарбитал убирают постепенно, но обычно его пьют после выписки не менее 3 месяцев.
Прогноз и последствия
У взрослых прогноз зависит от степени поражения мозга патологией. Самыми частыми последствиями перинатальной ГИЭ являются:
- задержка в развитии ребенка;
- дисфункции мозга в плане внимания, сосредоточенности на обучении;
- нестабильная работа внутренних систем организма;
- эпилептические припадки;
- гидроцефалия;
- вегетососудистая дистония.
Не нужно думать, что это приговор, даже разлад в центральной нервной системе корректируют, обеспечивая нормальную жизнь пациентам. Треть людей с этим расстройством излечивается полностью.
Профилактика
Если речь идет о взрослых, то все профилактические мероприятия должны быть направлены на полный отказ от вредных привычек. При этом нужно регулярно заниматься спортом, избегая чрезмерных нагрузок, правильно питаться, проходить регулярные медицинские осмотры, чтобы выявить опасные патологии на ранней стадии для их успешного купирования.
От травм никто не застрахован, но если более осторожно себя вести, то и их можно минимизировать.
Снизить риск ГИЭ у новорожденного может только его мама еще в период беременности. Для этого нужно:
- строго следить за режимом дня и личной гигиеной;
- отказаться от никотина и алкоголя даже в минимальной дозировке;
- проходить вовремя обследования у врачей и диагностику, особенно у невролога;
- доверить роды только квалифицированному персоналу.
Гипоксически-ишемическая энцефалопатия опасная болезнь, но ее можно предотвратить, и даже вылечить, но только если помощь была оказана вовремя и в дальнейшем врачебные рекомендации не нарушаются.
Pb #8: Что такое и как мы боялись гипоксически-ишемическогого поражения ЦНС
Автор: 4mam
Дата записи
Восьмая неделя жизни. Новые достижения моей мелкой в физическом развитии и играх, очень радовали папу и маму. Правда и попереживать тоже пришлось… На осмотре у невропатолога нам поставили диагноз — гипоксически-ишемическое поражение центральной нервной системы (ЦНС).
Еще о коликах
Разобравшись с причинами появления и лечением колик (о них я писал в предыдущем выпуске Papablog-a), стало немного легче.
Оказывается вместо дорогих лекарств с симетиконом, можно давать ребенку обычную воду или чай с фенхеля. Кто-бы что не говорил, но это работает (по крайней мере сработало у нас).
«Квалифицированный специалист»
Казалось бы родил ребеночка, да радуйся, да воспитывай. Но, как показывает практика, это не совсем так. Уже столько всего пережито в предыдущих выпусках: и роды с выпиской, и желтушка, и проверка врожденных рефлексов, и увеличение лактации, и первое купание, и выбор смеси, да этот список можно продолжать и продолжать. Кажется, папа знает уже все
На самом деле нет, не все…
Не помню, или рассказывал раньше, но после родов в левом глазу у ребенка появилось маленькое красное пятнышко (похожее на лопнувший сосуд). Сначала мы особо не придали этому значения, в роддоме сказали пройдет со временем.
Но шла уже 8 неделя, поэтому решили обратиться к невропатологу. Он поставил нам диагноз и назначил лечение. Но прочитав что такое гипоксически-ишемическое поражение, мы с женой засомневались в компетентности «специалиста». Пришлось даже учебники по неонатологии (раздел медицины который изучает младенцев и новорожденных) поднимать. И вот что мы нашли.
Гипоксически-ишемическая энцефалопатия
Почему раздел называется гипоксически-ишемическая энцефалопатия (ГИЭ) а не гипоксически-ишемическое поражение ЦНС? Да потому что, как оказалась, это одна и та же патология нервной системы. Правда второе сочетание встречается при более тяжелых формах, а первое при легких.
Что это такое
ГИЭ (гипоксически-ишемическая энцефалопатия) — это термин который объединяет в себе разные (и даже неуточненные) по происхождению поражения головного мозга, которые возникают до и во время родов. Различают три степени протекания ГИЭ в остром периоде:
Зачастую самой распространенной причиной поражения мозга является нехватка кислорода (гипоксия) до, или во время родов.
До родов (внутриутробная гипоксия) бывает:
- Гипоксемической (нехватка кислорода в крови).
- Гемической (падение гемоглобина в крови).
- Циркуляторной (нарушение кровотока).
- Тканевой (нарушения окислительных процессов в тканях плода).
Причинами способствующими внутриутробной гипоксии плода могут стать:
- Тяжелые соматические болезни матери (заболевания сердца, сосудов, дыхательных путей и т. д.).
- Перенесенные патологии во время беременности (угроза выкидыша, длительные токсикозы и т.д.).
- Эндокринные заболевания (сахарный диабет).
- Наличие различных инфекций во время беременности.
- Наличие вредных привычек у мамы.
- Генетечиские, хромосомные патологии.
- Иммунологические отклонения в системе мать — плацента — плод.
- Многоплодная беременность.
Во время родов (по научному: интранатальный период) причинами развития гипоксии могут быть:
- Аномальное предлежание плода.
- Оперативное родоразрешение (а именно применение щипцов, вакуум-экстрактора, кесарево сечение, особенно экстренное).
- Острая гипоксия при родах у матери (может быть связана даже с шоком).
- Нарушения плацентарно-плодового кровообращения (тугое обвитие пуповиной, выпадение петель, ущемление и т. д.).
- Разрыв матки.
- Продолжительность родов (затяжные, быстрые, стремительные).
- Предлежание или преждевременная отслойка плаценты.
В чем опасность и как проявляется заболевание
Многие родители увидев диагноз ГИЭ (собственно как и мы с женой) очень переживают по этому поводу. Как это отразится на последующем развитии ребенка, будет ли малыш ходить, ползать, не будет ли отличаться от других детей и тд.
Как уже упоминалось выше есть 3 степени поражения головного мозга.
- При легкой степени могут наблюдаться минимальные изменения в двигательной и рефлекторной сферах (гипервозбудимость или угнетение) которые сохраняются не более 7 дней. Проявляться отклонения могут в виде эмоционального или двигательного беспокойствия: повышение спонтанной активности, проявление тремора (содрогания) конечностей, оживление коленных и безусловных рефлексов, снижение основных рефлексов (Моро, Бабкина, Бауэра, Робинсона). Обычно данные отклонения проходят в первые 5-7 дней жизни, в некоторых случаях, их даже не рассматривают как патологию.
- При среднетяжелой степени угнетения и возбуждения ЦНС наблюдаются 7 и более дней. У детей заметны вялость, уменьшение двигательной активности, снижение и повышение (обычно сначала понижение, а потом повышение) мышечного тонуса в мышцах сгибателях. Проявляются спонтанные вздрагивания и судорожные подергивания. Основные рефлексы снижаются, возможно проявление анизокории (разные размеры зрачков), опущение верхнего века, косоглазия, колебания глаз с высокой частотой. Также у ребенка могут наблюдаться частые срыгивания, мраморная кожа (неравномерный окрас) сердечная аритмия. Обычно данные расстройства сохраняются до 2-4 месяцев жизни. (Благо у моего ребенка ничего такого не наблюдалось).
- При тяжелой степени ГИЭ (ее как раз и называют гипоксически-ишемическое поражение ЦНС) могут диагностироваться мозговая кома, снижение или пропадание мышечного тонуса, редкие мигания, отсутствие сосания и глотания, наличие судорог, сбои в дыхание. Обычно тяжелое состояние может продолжаться 1.5 -2 месяца, зачастую после такой болезни у ребенка могут остаться серьезные нарушения ЦНС.
Диагноз и диагностика: стоит ли волноваться?
Обязательно перед походом к врачу, узнайте хоть какие то отзывы о нем.
Самое интересное, есть как минимум 2 причины по которым невропатолог не мог поставить диагноз:
- Диагноз энцефалопатия новорожденных может быть поставлен только в течении 1-го месяца жизни (моей уже почти 2). С указанием основной причины и характера изменений головного мозга.
- В грудном возрасте (после 28 дней с рождения) чтобы поставить такой диагноз нужно привести перечень основных клинических синдромов с указанием причины их возникновения (задержка моторного развития, психического, эпилепсия и т. д.).
Диагностика поражений основывается на:
- Изучении данных протекания беременности и родов.
- Оценке ребенка по шкале Апгар.
- Анализах и обследованиях (компьютерная томография, допплеровская энцефалографии и т. д.).
Как лечится ГИЭ
Обычно лечение проходит комплексно (лекарственная терапия, ЛФК и лечебный массаж, занятия с логопедом, физиотерапевтические процедуры). Конечно как лечить ГИЭ, может сказать только врач. Хотя они учатся по учебникам, и все формы и лечение вплоть до дозировки прописаны в книгах, лучше обратиться к специалисту (грамотному специалисту). Сходив на прием к другому невропатологу, диагноз не подтвердился. Хотя я это уже и так знал 🙂
Что такое ПЭП
Как пишет доктор Комаровский, педиатры стран СНГ ставят диагноз ПЭП (перинатальная энцефалопатия), когда не знают что делать.
В международной классификации болезней (МКБ) такой болезни нет. В своей книге он отмечает, что дословно ПЭП переводится как болезнь мозга (без уточнения причины). И само по себе понятие существовать не может. Неудивительно что в роддомах и детских неврологических центрах, а также отделениях детский патологий, данный диагноз не встречается.
Неврологический диагноз связанный с нарушениями работы головного мозга, требует особого лечения (например ГИЭ (гипоксически-ишемическая энцефалопатия). А если вам написали что у вас ПЭП и прописали таблетки (кстати в большинстве случаев они не нужны), тогда волноваться не стоит, поводов для беспокойства нет. Как говорит доктор: «Это мелочи, само пройдет, образуется, перерастется».
Развитие доченьки
Восьмая неделя. Время прогулок, сна и бодрствования почти не изменилось, но вот по сравнению с предыдущей неделей у дочи явно улучшился аппетит. Накормив ребенка как обычно, (докармливали мы 30 мл смеси) молодые мама и папа начали замечать что по истечению 30 минут (иногда 1 часа) мелкая начинала плакать. Не помогало ничего кроме «добавки». Тогда мы и приняли решение увеличить «норму» и с 8-й недели, после кормления грудью, давали уже 60 мл детского питания.
Также явно был заметен прогресс в держании головы лежа на животике. Время удержания колебалось уже порядка 40-60 секунд (а иногда и более). Что не могло не радовать отцовское сердце, доча растет 🙂
Первые игры которые описывал в Papablog-е #5 видоизменились, ребенок следил за погремушками уже не просто водя глазами. Моя кроха уже научилась поворачивать головку по направлению за игрушкой. Правда на звук пока так и не реагировала, я очень переживал по этому поводу. Поэтому нашел способ проверить слух, но об этом уже в следующем выпуске.
Завершилась восьмая неделя, второй месяц жизни подходит к концу. На следующей седмице нас ожидает плановый осмотр у педиатра (будет интересно узнать какого роста и сколько весит моя мелкая), а также стандартные прогулки, кормления, купания, игры и упражнения для развития.
До новых встреч на Papablog-е, впереди мои впечатления и эмоции, и конечно же, способности новорожденной доченьки.
Гипоксически-ишемическая энцефалопатия
Постгипоксическая энцефалопатия – это серьезное поражение оболочек мозга невоспалительного характера, которое диагностируется у новорожденных. Патология развивается из-за гипоксии плода.
Причины патологии
Постгипоксическая энцефалопатия не является редким заболеванием. Гипоксия, перенесенная плодом, вызывает кислородное голодание мозга, в результате чего происходит гибель некоторого количества нейронов. В период вынашивания ребенка гипоксию могут спровоцировать следующие факторы:
- сердечная недостаточность у женщины;
- сахарный диабет 1 или 2 типа у матери;
- токсическое воздействие алкоголя, никотина, наркотических веществ;
- несовместимость резус-фактора матери и плода;
- многоплодная беременность.
Гипоксию часто переносят дети, рожденные переношенными. Еще один фактор, провоцирующий кислородное голодание плода – это угроза срыва или преждевременные роды.
Заболевание может развиться непосредственно в процессе родов по следующим причинам:
- сильная кровопотеря;
- неправильное положение плода;
- обвитие;
- стимуляция родовой деятельность;
- преждевременный прокол пузыря.
Таким образом, причины развития патологии у детей могут быть обусловлены как внутриутробным развитием, так и осложненными родами или родовой травмой.
При гипоксически-ишемической энцефалопатии у новорожденных (ГИЭ) в первую очередь диагностируется асфиксия – состояние удушья, при котором младенец не может сделать первый вдох.
Приобретенная энцефалопатия проявляется в первую недели жизни ребенка. Она может быть спровоцирована врожденным пороком сердца или нарушением дыхательной функции.
Особенности развития и симптомы
Головной мозг является важнейшей частью центральной нервной системы человека. Кислородное голодание приводит к недостатку кислорода в тканях мозга, в результате чего нарушается нормальный кровоток и замедляются метаболические процессы. Недостаток питания приводит к отмиранию нейронов некоторых участков мозга, что чревато развитием ряда неврологических нарушений.
Нарушение кровообращения в тканях головного мозга новорожденного влечет за собой быстрое нарастание отека. Отечность тканей провоцирует повышение давления, в результате чего и происходит гибель нейронов.
Опытный врач распознает симптомы гипоксической энцефалопатии в первые минуты после появления ребенка на свет. О нарушении функционирования нервной системы свидетельствуют следующие симптомы:
- слабый или запоздалый первый крик новорожденного;
- снижение рефлексов;
- капризность, постоянный плач;
- синеватый оттенок кожи.
Диагностика гипоксической энцефалопатии, как правило, проводится в первый часы после появления на свет.
Формы патологии
В зависимости от степени поражения нервной системы, различают три степени тяжести болезни у младенцев:
- легкая;
- средняя;
- тяжелая степени энцефалопатии.
Легкая форма заболевания характеризуется нарушением сна, проблемами с засыпанием и пробуждением, легкой беспокойностью и подергиванием подбородка. У ребенка наблюдается повышенная рефлекторная деятельность. Малыш беспокоен, часто беспричинно вскрикивает и плохо спит. Для этой формы характерно беспричинное повышение двигательной активности, с одновременным снижением глотательного и сосательного рефлексов. Заболевание успешно лечится в первые несколько недель после рождения и в дальнейшем не оставляет негативных последствий.
При гипоксической энцефалопатии средней степени тяжести наблюдаются следующие симптомы:
- слабость естественных врожденных рефлексов;
- неврологические нарушения локального характера;
- ослабление мышц тела;
- беспокойство, частые крики без причины.
Неврологические нарушения при средней степени тяжести болезни характеризуются косоглазием, птозом, ослаблением века.
Тяжелая форма гипоксической энцефалопатии у младенцев сопровождается следующими симптомами:
- частые судорожные состояния приступообразного характера;
- полное отсутствие рефлексов, характерных для новорожденных;
- критически сниженное артериальное давление;
- слабый пульс;
- полное отсутствие мышечного тонуса.
Тяжелая форма патологии может сопровождаться нарушением работы различных внутренних органов.
Лечение патологии
Лечение назначается в зависимости от степени патологии. Причиной легкой степени энцефалопатии является нарушение мозгового кровообращения, поэтому все симптомы благополучно исчезают при нормализации кровообращения. Причиной заболевания средней степени тяжести является отек тканей и последующее повышение внутричерепного давления.
Лечение средней и тяжелой степени болезни основано на приеме следующих препаратов:
- противосудорожные препараты;
- лекарства для стимуляции работы сердечно-сосудистой системы;
- противоотечные препараты.
Медикаментозное лечение включает большой перечень препаратов и подбирается индивидуально для каждого случая болезни у новорожденных.
Сразу после рождения, ребенка помещают в кувез. Малышам с такой патологией противопоказано тугое пеленание, громкие звуки и яркий свет. Малыш обязательно содержится при температуре не ниже 25 0 С. В большинстве случаев, новорожденным устанавливается система для вентиляции легких.
Ребенок содержится в стационаре длительное время. Состояние здоровья малыша требует тщательного контроля на протяжении как минимум первых двух недель жизни. В дальнейшем решение о продлении лечения в стационаре принимается врачом, в зависимости от тяжести поражения мозга у пациента.
Целью лечения в стационаре является:
- насыщение тканей кислородом;
- нормализация дыхательной функции;
- снятие отечности тканей мозга;
- нормализация внутричерепного давления.
В дальнейшем после снятия острых симптомов, ребенку показан курс физиотерапевтических процедур для нормализации всех метаболических процессов головного мозга.
После выписки из стационара лечение продолжается в домашних условиях с обязательным осмотром врачом каждые три-четыре дня. Так как при энцефалопатии часто развиваются судорожные припадки, прием противосудорожных препаратов может продолжаться вплоть до полугода, в зависимости от тяжести симптомов.
Домашнее лечение во многом зависит от того, как малыш развивается. Если задержек в развитии нет, а судорожные припадки больше не повторяются, ребенку достаточно регулярного осмотра неврологом, без дополнительного лечения дома.
При обширном повреждении центральной нервной системы, лечение продолжается длительно и корректируется, в зависимости от состояния пациента.
Возможные последствия и прогноз
Наиболее благоприятен прогноз при легкой степени заболевания. В этом случае терапия включает насыщение крови кислородом и стимуляцию нормального мозгового кровообращения. Как правило, тревожные симптомы успешно проходят в первую недели жизни малыша. Негативных последствий и неврологических нарушений при этом не наблюдается.
Во всех остальных случаях существует риск развития следующих последствий:
- нарушение развития ребенка;
- нарушение функции мозга;
- нарушение работы некоторых внутренних органов;
- местные неврологические нарушения;
- гидроцефалия;
- вегетативная дисфункция;
- эпилепсия.
Нарушение функции мозга в дальнейшем может проявляться неспособностью длительной концентрации внимания и ослаблением памяти. Высока вероятность, что такой ребенок будет плохо учиться из-за неусидчивости.
Нарушения развития могут проявляться логопедическими нарушениями и замедлением роста. В этом случае малышу показано лечение в специальных медицинских учреждениях.
Нарушение работы некоторых внутренних органов требует тщательного отслеживания симптомов и своевременного лечения при их обострениях. От этой проблемы можно избавиться только в том случае, если своевременно обратить внимание на тревожные симптомы.
Гидроцефалия вследствие энцефалопатии требует своевременного лечения, в том числе и хирургического. Это заболевание также может стать причиной ряда неврологических нарушений.
При энцефалопатии тяжелой степени высок риск дальнейшего развития эпилепсии. Это связано с нарушением работы некоторых участков мозга и отмиранием нейронов, в результате чего у больных наблюдается повышение возбудимости определенных участков мозга и, как следствие, судорожные припадки. Тем не менее, своевременно начатое лечения приобретенной эпилепсии зачастую позволяет успешно избавиться от судорожных припадков.
Как избежать заболевания
Серьезный подход к планированию беременности и тщательное обследование матери во время вынашивания ребенка – это гарантия успешного течения беременности и отсутствия осложнений у новорожденного малыша. Женщины с хроническими заболеваниями, такими как эпилепсия или диабет, должны пройти комплексное обследование до зачатия ребенка. Добившись компенсации собственного заболевания перед зачатием, каждая женщинам имеет высокий шанс выносить и родить абсолютно здорового малыша.
Так как причиной патологии у младенцев является гипоксия во внутриутробном периоде, долг каждой женщины заключается в отказе от вредных привычек во время вынашивания ребенка.
Избежать осложнений во время родов поможет тщательное обследование и ведение беременности квалифицированным врачом.