Давление плато это
Медицина легких
Давление в конце плато
Давление в конце плато (Pplat) тесно коррелирует с альвеолярным давлением и отражает эластическое состояние легких (9). В настоящее время его широко используют для расчета статической податливости легких Cst:
Разница между Ppeak и Pplat отражает резистивное состояние воздухоносных путей; ее используют для расчета инс-пираторного сопротивления дыхательных путей Rinsp:
Мониторинг этих показателей имеет большое значение для динамического наблюдения за состоянием легких в процессе интенсивной терапии.
Неоспоримо замечание В.Л. Кассиля (13), что при нисходящей форме потоковой кривой «включение инспираторной паузы удлиняет фазу вдоха, но мало изменяет форму кривой давления». При данном виде кривой поток в конце вдоха приближается к нулю и в определенной степени моделирует паузу вдоха, в конце которой уже практически закончено распределение газа в легких.
Пауза вдоха считается средством, позволяющим улучшить распределение поданного ДО (Vr), снизить повышенное РаС02 и увеличить Ра02 (за счет вовлечения в газообмен большей части легких), улучшить вентиляционно-пер-фузионное соотношение и уменьшить объем мертвого пространства (VD/V,) (3, 6, 13, 15, 151). Газовая смесь успевает заполнить «медленные» зоны легких с высокой временной константой. Во время инспираторной паузы может проявляться эффект Пендельлюфта (Pendelluft), когда при выравнивании давления между зонами легких с различной степенью патологических изменений происходит перераспределение потока из быстро заполняющихся участков легких (малая временная константа) в медленно заполняющиеся зоны с большой временной константой. Эффект Пендельлюфта имеет и отрицательную сторону, особенно при длительной паузе вдоха: в медленно расправляющихся отделах легких происходит перераспределение воздуха, который уже участвовал в газообмене и поэтому обеднен кислородом. Парциальное давление кислорода в нем относительно низкое, что делает малоэффективным участие этой порции воздуха в оксиге-нации.
Происходит также коллатеральная вентиляция в дистальных отделах легких через каналы в стенках альвеол (поры Кона) и через коммуникации между бронхиолами (каналы Ламберта).
Не следует забывать, что достаточно длинная пауза вдоха (более 0,5 с) может существенно влиять на увеличение среднего давления Pmean в дыхательных путях (и, следовательно, внутригрудно-го давления) с соответствующими отрицательными гемодинамическими эффектами. При ИВЛ с инспираторной паузой показан мониторинг величины Pmean, с тем чтобы своевременно заметить его чрезмерное повышение и предпринять определенные действия.
Пиковое давление вдоха (PIP)
Большинство осложнений, связанных с ИВЛ, обусловлены неправильным подбором PIP.
снижение сердечного выброса;
повышение легочного сосудистого сопротивления.
PIP подбирают в зависимости от:
эффективного ДО (объёма выдоха); Наиболее приемлемы в острую фазу заболевания легких — 4-6 мл/кг.
величины экскурсий грудной клетки;
аускультативной картины, интенсивности дыхательных шумов;
Положительное давление в конце выдоха (РЕЕР, ПДКВ)
Основные положительные эффекты:
улучшает вентиляционно-перфузионные отношения;
перемещает жидкость из альвеолярного в интерстициальное пространство;
препятствует спадению альвеол и мелких дыхательных путей;
В острой фазе РДС обычно применяют РЕЕР 4-6 см вод ст. У новорождённых с РДС такая величина РЕЕР обычно не оказывает отрицательного влияния на легочную механику и сердечно-сосудистую систему.
Потенциальные отрицательные эффекты высокого РЕЕР:
снижение венозного притока к сердцу;
повышение легочного сосудистого сопротивления;
перераспределение легочного кровотока в невентилируемые альвеолы;
Исследования, проведённые в 80-х годах прошлого века, показали, что повышение ЧД более 60 в мин приводит к лучшей синхронизации пациента с дыханием вентилятора, улучшает обмен газов в легких и снижает частоту баротравмы. При не медикаментозной синхронизации дыхания пациента и вентилятора, в острую фазу РДС, иногда используют ЧД 80-120 в мин (Твд 0.3 с). Однако необходимо помнить, что подобная стратегия может приводить к гипервентиляции с дыхательным алкалозом, отрицательными последствиями которой будут:
Снижение сердечного выброса.
Спазм мозговых сосудов.
Нарушение вентиляционно-перфузионных отношений.
В режиме А/С больной сам выбирает частоту принудительного дыхания, что является определённым преимуществом этого режима.
В настоящее время более важными считаются абсолютные величины Твд и Твыд, а не их соотношение. Минимальное Твд должно быть таково, чтобы пациент получил необходимый дыхательный объём, а короткое Твыд не должно приводить к появлению auto-PEEP. Учитывая короткую константу времени у больных РДС, вполне адекватным Твд будет 0.35 с, а у детей массой менее 1000 г менее 0.3 с. При превышении ЧД 60 в мин, для контроля за возможным развитием «auto-PEEP» желательно иметь графический монитор.
Особенности обеспечения синхронности дыхания пациента и аппарата ИВЛ.
У большинства новорождённых при проведении ИВЛ сохраняется спонтанное дыхание, но часто не синхронное с принудительными вдохами вентилятора. Сохранение самостоятельного дыхания чаще всего положительно влияет на обмен газов в легких и гемодинамику, но может и снижать эффективность ИВЛ. Это происходит, если новорождённый дышит:
1) с частотой дыхания отличной от установленной на вентиляторе и/или 2) с нерегулярным ритмом дыхания, а также в том случае если частота дыхания пациента и вентилятора одинаковы, но 3) не совпадают фазы вдоха и выдоха. Как правило, новорождённый форсированно дышит или «борется» с респиратором, если аппарат ИВЛ не обеспечивает ему адекватную минутную вентиляцию. Т.к. известно, что минутная вентиляция равна произведению дыхательного объёма на частоту, синхронизировать пациента с аппаратом ИВЛ можно, увеличив частоту респиратора или дыхательный объём (Piр), в случае если последний не превышает 6-7 млкг.
Существует два основных способа достижения синхронности дыхания пациента и вентилятора: перевод на принудительную ИВЛ (IMV) и пациент-триггерная вентиляция.
При IMV синхронизация достигается глубокой седатацией или миорелаксацией. Каждый из этих методов имеет свои специфические недостатки:
— Депрессия сердечно-сосудистой системы.
Увеличение продолжительности ИВЛ.
Увеличение продолжительности ИВЛ.
Спонтанное дыхание во время ИВЛ периодически снижает внутригрудное давление и способствует венозному притоку к сердцу, наполнению правого и левого желудочков, повышает сердечный выброс.
Принудительная вентиляция легких является оправданной только у пациентов:
с грубыми неврологическими нарушениями и т. н. «гипервентиляционным» синдромом, когда неконтролируемо высокая частота самостоятельных дыханий больного приводит к грубой гипервентиляции
с декомпенсированным метаболическим ацидозом
с сохраняющейся на пациент — триггерной вентиляции гипоксемией.
В остальных случаях предпочтительнее использовать пациент-триггерную вентиляцию.
Особые указания. При подборе параметров необходимо помнить, что:
1. Основными агрессивными параметрами ИВЛ, которые следует снижать в первую очередь, являются: PIP и FiO2 (> 40%).
2. За один раз давление меняется не более чем на 1-2смН2О, а частота не более чем на 5 вдохов. Лишь FiO2 может меняться под контролем SatO2 (88-92%) ступенчато на 5-10%.
Чурсин В.В. Искусственная вентиляция легких (учебно-методическое пособие)
Информация
Физиология дыхания
Проводящие пути
Нос — первые изменения поступающего воздуха происходят в носу, где он очищается, согревается и увлажняется. Этому способствует волосяной фильтр, преддверие и раковины носа. Интенсивное кровоснабжение слизистой оболочки и пещеристых сплетений раковин обеспечивает быстрое согревание или охлаждение воздуха до температуры тела. Испаряющаяся со слизистой оболочки вода увлажняет воздух на 75-80%. Длительное вдыхание воздуха пониженной влажности приводит к высыханию слизистой оболочки, попаданию сухого воздуха в легкие, развитию ателектазов, пневмонии и повышению сопротивления в воздухоносных путях.
Трахея — основной воздуховод, в ней согревается и увлажняется воздух. Клетки слизистой оболочки захватывают инородные вещества, а реснички продвигают слизь вверх по трахее.
Бронхи (долевые и сегментарные) заканчиваются концевыми бронхиолами.
В альвеолах происходит газообмен между кровью легочных капилляров и воздухом. Общее число альвеол равно примерно 300 млн., а суммарная площадь их поверхности — примерно 80 м 2 . Диаметр альвеол составляет 0,2-0,3 мм. Газообмен между альвеолярным воздухом и кровью осуществляется путем диффузии. Кровь легочных капилляров отделена от альвеолярного пространства лишь тонким слоем ткани — так называемой альвеолярно-капиллярной мембраной, образованной альвеолярным эпителием, узким интерстициальным пространством и эндотелием капилляра. Общая толщина этой мембраны не превышает 1 мкм. Вся альвеолярная поверхность легких покрыта тонкой пленкой, называемой сурфактантом.
при низком давлении растяжения, уменьшает действие сил, вызывающих накопление жидкости в тканях. Кроме того, сурфактант очищает вдыхаемые газы, отфильтровывает и улавливает вдыхаемые частицы, регулирует обмен воды между кровью и воздушной средой альвеолы, ускоряет диффузию СО2, обладает выраженным антиокислительным действием. Сурфактант очень чувствителен к различным эндо- и экзогенным факторам: нарушениям кровообращения, вентиляции и метаболизма, изменению РО2 во вдыхаемом воздухе, загрязнению его. При дефиците сурфактанта возникают ателектазы и РДС новорожденных. Примерно 90-95% альвеолярного сурфактанта повторно перерабатывается, очищается, накапливается и ресекретируется. Период полувыведения компонентов сурфактанта из просвета альвеол здоровых легких составляет около 20 ч.
2. Резервный объем вдоха (РОвд – IRV – Inspiratory Reserve Volume) — объем, который может дополнительно поступить после спокойного вдоха, т.е. разница между нормальной и максимальной вентиляцией. Нормальное значение: 2-2,5 л (около 2/3 ЖЕЛ).
увеличением скорости потока (форсирование вдоха или выдоха) сопротивление дыхательных путей увеличивается.
Сопротивление дыхательных путей зависит также от объема легких. При большом объёме паренхима оказывает большее «растягивающее» действие на дыхательные пути, и их сопротивление уменьшается. Применение ПДКВ (PEEP) способствует увеличению объема легких и, следовательно, снижению сопротивления дыхательных путей.
Сопротивление дыхательных путей в норме составляет:
4. Повышенная вентиляция — любое увеличение альвеолярной вентиляции по сравнению с уровнем покоя, независимо от парциального давления газов в альвеолах (например, при мышечной работе).
12.Асфиксия — остановка или угнетение дыхания, связанные, главным образом, с параличом дыхательных центров или закрытием дыхательных путей. Газообмен при этом резко нарушен (наблюдается гипоксия и гиперкапния).
В целях диагностики целесообразно различать два типа нарушений вентиляции — рестриктивный и обструктивный.
Острая дыхательная недостаточность
Классификация ОДН
В соответствии с вышеизложенным (с позиции оказания экстренной помощи), в первую очередь нужно классифицировать ОДН по тяжести.
Наиболее удобно в реаниматологии классифицировать все синдромы, связанные с органной недостаточностью (точнее – с функциональной недостаточностью того или иного органа) по степени компенсации – способности выполнять свои функции. Любую недостаточность можно разделить на компенсированную, субкомпенсированную и некомпенсированную.
Взяв для аналогии классификации Дембо А.Г. (1957), Rossier (1956), Малышева В.Д. (1989) можно разделить ОДН на:
— Компенсированную, когда при умеренном напряжении функции дыхания поддерживается нормальный газовый состав крови и удовлетворяются метаболические потребности организма. Клинически в состоянии покоя ЧДД до 30 в мин, газы крови и КЩС в норме, ЖЕЛ снижено до 30-60 мл/кг. По Дембо — 1 вид, по Rossier – латентная, по Малышеву — I стадия. Сюда же можно отнести и состояния, при которых повышается потребность организма в кислороде в покое, хотя правильнее это состояние называть «компенсаторная ОДН».
— Субкомпенсированную, когда при выраженном напряжении функции дыхания поддерживается нормальный газовый состав крови и уже не полностью удовлетворяются метаболические потребности организма. Клинически в состоянии покоя ЧДД более 30 в мин, газы крови – РаО2 в норме или несколько снижено, РаСО2 может быть снижено, КЩС – метаболический ацидоз, ЖЕЛ менее 30 мл/кг. По Дембо — 2 вид, по Rossier – парциальная, по Малышеву — II стадия.
— Некомпенсированную, когда при выраженных нарушениях механики дыхания не поддерживается нормальный газовый состав крови и уже абсолютно не удовлетворяются метаболические потребности организма. Клинически в состоянии покоя ЧДД более 35 в мин или брадипноэ ( 1, увеличивается физиологическое мертвое пространство, сокращается площадь реального газообмена. Как итог, прогрессирует гипоксемия и гипоксия, которые невозможно компенсировать развивающимся тахипноэ. Для ТЭЛА, кроме того, характерны выраженные гемодинамические нарушения и явления правожелудочковой недостаточности, что усугубляет ситуацию.
Искусственная вентиляция легких
Однако на практике существенное отрицательное влияние ИВЛ на функцию почек наблюдается достаточно редко. Вероятно, положительное влияние на оксигенацию адекватно проводимой ИВЛ все-таки превалирует над отрицательным антидиуретическим эффектом. И в практике автора, и по данным литературы нередки случаи, когда при развивающейся олигурии на фоне гипоксии различного генеза (ОРДС, артериальная гипотен-зия, гестозы) перевод больных на ИВЛ (в комплексе с другой терапией) сопровождался увеличением диуреза вплоть до полиурии. Надо думать, это связано с устранением гипоксии, снижением уровня катехоламинов, купированием спазма артериол и т. д. Прогрессирование олигурии чаще всего обусловлено другой причиной (например, органическими изменениями почек, нескоррегированной гиповолемией, эндогенной или экзогенной интоксикацией).
Возможное отрицательное действие ИВЛ на функцию печени и ЖКТ связано со следующими механизмами:
Принципы работы аппаратов ИВЛ
Сущность работы любого приспособления или аппарата для проведения ИВЛ заключается в том, что необходимо сделать вдох — вдуть в лёгкие газовую смесь, и потом обеспечить выдох — возможность удаления из лёгких этой смеси.
Принципиальным моментом в обеспечении цикличной работы аппарата ИВЛ является способ переключения с вдоха на выдох и обратно.
Существуют несколько способов осуществления цикличности:
— По давлению – аппарат контролирует давление в дыхательном контуре и по заданным величинам давления в конце вдоха и выдоха обеспечивает цикличную ИВЛ. Принцип работы следующий – генератор сжатой газовой смеси (компрессор, турбина) осуществляет вдох – раздувает лёгкие, пока в них не поднимется давление, например до 18 см.вод.ст., после чего срабатывают клапана и лёгким пациента даётся возможность освободиться от избыточного давления, удалив отработанную газовую смесь и снизив давление, например до 0 см вод.ст. Затем опять начинается вдох, опять до достижения 18 см.вод.ст. и т.д. Изменяя величины давления для срабатывания клапанов и производительность генератора можно менять параметры ИВЛ – ДО, ЧД и МОД.
— По частоте – аппарат контролирует время фаз дыхательного цикла – вдоха и выдоха. Зная частоту дыхания и соотношения длительности фаз, можно рассчитать длительность вдоха и выдоха. Например, ЧД – 10 в минуту, значит на один дыхательный цикл (вдох+выдох) уходит 6 секунд. При соотношении вдох:выдох (I:E) – 1:2, длительность вдоха составит 2 секунды, выдоха 4 секунды. Принцип работы следующий – генератор сжатой газовой смеси (компрессор, турбина) осуществляет вдох – раздувает лёгкие в течении 2-х секунд, после чего срабатывают клапана и лёгким пациента даётся возможность освободиться от отработанной газовой смеси в течении 4-х секунд. Изменяя ЧД (и/или I:E) и производительность генератора можно менять ДО и МОД.
— По объёму – аппарат контролирует объём газовой смеси, нагнетаемой в лёгкие пациента, обеспечивая ДО. Затем даётся время для освобождения от отработанной газовой смеси. Изменяя ДО и производительность генератора (МОД), при заданном соотношении I:E, можно изменять ЧД.
Достаточно давно появился (ещё в РО-5), но только сейчас широко используется ещё один принцип управления цикличностью:
— По усилию пациента – когда сам больной инициирует вдох и генератор нагнетает в его лёгкие заданный ДО. В этом случае такие показатели как ЧД и, соответственно МОД, определяются самим пациентом. Эти триггерные (откликающиеся) системы определяют попытки самостоятельного вдоха а) по созданию небольшого отрицательного давления в дыхательном контуре или б) по изменению потока газовой смеси.
В более современном представлении классификацию по принципу обеспечения цикличности можно представить в следующем виде:
— Аппараты или режимы ИВЛ с контролем дыхательного объёма. Работая «по частоте», т.е. в рамках расчётного времени на вдох, аппарат рассчитывает с какой скоростью надо доставить заданный ДО в лёгкие пациента.
— Аппараты или режимы ИВЛ с контролем давления на вдохе. Работая также «по частоте», т.е. в рамках расчётного времени на вдох, аппарат с определённой скоростью и до достижения установленного давления в дыхательных путях, нагнетает в лёгкие пациента ДО, измеряя его величину.
Высокое давление в дыхательных путях при ИВЛ
Высокое давление в дыхательных путях при ИВЛ
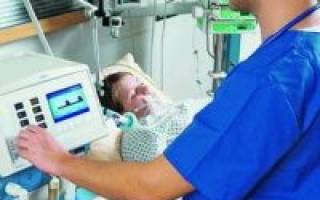
Давление в дыхательных путях — чувствительный параметр, контролируемый во время механической вентиляции легких. Монитор давления в дыхательных путях может быть установлен в аппарате, совмещен с абсорбером углекислого газа, находиться в разветвлении контура или около клапана вдоха со стороны пациента (оптимальное расположение). При последнем месторасположении можно выявить высокое, низкое или не меняющееся давление в дыхательных путях, что при двух других вариантах расположения может быть пропущено. При нахождении в области разветвления контура в случае обструкции инспираторного сегмента циркуляционного контура отмечается понижение пикового давления на вдохе, при обструкции экспираторного сегмента контура возникает повышение нижней точки и пикового давления в дыхательных путях. Для удобства в циркуляционном дыхательном контуре давление в дыхательных путях часто определяют в абсорбере углекислого газа. При таком расположении обструкция в любой части дыхательного контура (инспираторной или экспираторной) приведет к повышению пикового давления в дыхательных путях без изменения давления в нижней точке.
Высокое давление в дыхательных путях при ИВЛ: причины
A. Пиковое давление в дыхательных путях повышается при кашле, обструкции контура (обычно на уровне эндотрахеальной трубки), большом дыхательном объеме. В старых типах наркозных аппаратов повышение скорости потока газа приводит к повышению доставляемого дыхательного объема, особенно когда установлен небольшой дыхательный объем (например, у детей).
Б. Обструкция инспираторного сегмента дыхательного контура происходит вследствие различных причин, например при нарушении направления потока (при неправильной установке увлажнителя). При обструкции канала вдоха контура отмечается повышение пикового давления в дыхательных путях, если давление измеряется проксимальнее места обструкции (например, в абсорбере углекислого газа), и отмечается понижение давления в дыхательных путях, если давление измеряется дистальнее места обструкции (например в области разветвления контура)
B. Давление при инспираторной паузе (статическое давление в дыхательных путях во время задержки дыхания на вдохе) помогает дифференцировать повышенное сопротивление дыхательных путей и пониженную податливость грудной клетки (рисунок ниже, верхние графики). Пониженная податливость грудной клетки повышает уровень давления плато, тогда как при повышении сопротивления дыхательных путей уровень давления во время паузы понижен или не изменяется. Разница между давлением во время паузы и пиковым давлением в норме составляет 4-8 см водн. ст., оказывается больше при возрастании сопротивления дыхательных путей, так как увеличение пикового давления в данном случае происходит без сопутствующего повышения давления во время паузы.
Давление в дыхательных путях (верхние графики) и поток (нижние графики) помогает дифференцировать проблемы, связанные с низким комплайнсом и высоким сопротивлением. В норме разница между пиковым давлением и давлением во время паузы составляет 4-8 см водн. ст. Понижение комплайнса вызывает пропорциональное повышение обоих давлений, тогда как при увеличении сопротивления дыхательных путей возрастает только пиковое давление. Снижение комплайнса грудной клетки вызывает повышение пикового экспираторного потока и укорочение продолжительности экспираторного потока. При повышении сопротивления дыхательных путей, наоборот, снижается пиковый экспираторный поток и увеличивается длительность фазы выдоха.
Инспираторная пауза может создаваться некоторыми анестезиологическими вентиляторами, или вручную путем кратковременной окклюзии экспираторной части контура в начале выдоха. Такой ручной метод может быть использован, только если давление в дыхательных путях определяется в области разветвления контура. Скорость экспираторного потока также помогает дифференцировать повышения сопротивления от нарушений податливости. Скорость экспираторного потока можно качественно оценить путем наблюдения за скоростью подъема меха аппарата или с помощью аускультации длительности выдоха. Лучше всего его измерять спирометром, расположенным вблизи дыхательных путей или в экспираторной части дыхательного контура (рисунок выше, нижние кривые).
Г. Уменьшенная площадь поперечного сечения мелких или крупных дыхательных путей или эндотрахеальной трубки повышает сопротивление потоку. Для выявления уровня обструкции выслушивайте экспираторные шумы и наблюдайте за формой капнограммы. Обструкция мелких дыхательных путей (бронхоспазм или хроническая обструктивная болезнь легких (ХОБЛ)) сопровождается экспираторными хрипами и скошенной формой альвеолярного плато капнограммы, которая обусловлена неравномерностью альвеолярной вентиляции. Обструкция крупных дыхательных путей (инородное тело в бронхе) или эндотрахеальной трубки (перегиб эндотрахеальной трубки) не сопровождается хрипами на выдохе или неравномерностью альвеолярной вентиляции. Наличие слизи или крови в дыхательных путях может создавать характерные слышимые свистящие хрипы, но не вызывает сглаживание альвеолярного плато на капнограмме.
Стоит отметить, что любой вид обструкции ведет к гипоксии, которая в свою очередь вызывает повреждение головного мозга и аритмии. Именно поэтому в стандарт мониторинга во время анестезии входит мониторинг ЭКГ электрокардиографами (из этого источника можно узнать подробнее о таком оборудовании) или кардиомониторами.
Пиковое давление вдоха (PIP)
Большинство осложнений, связанных с ИВЛ, обусловлены неправильным подбором PIP.
снижение сердечного выброса;
повышение легочного сосудистого сопротивления.
PIP подбирают в зависимости от:
эффективного ДО (объёма выдоха); Наиболее приемлемы в острую фазу заболевания легких — 4-6 мл/кг.
величины экскурсий грудной клетки;
аускультативной картины, интенсивности дыхательных шумов;
Положительное давление в конце выдоха (РЕЕР, ПДКВ)
Основные положительные эффекты:
улучшает вентиляционно-перфузионные отношения;
перемещает жидкость из альвеолярного в интерстициальное пространство;
препятствует спадению альвеол и мелких дыхательных путей;
В острой фазе РДС обычно применяют РЕЕР 4-6 см вод ст. У новорождённых с РДС такая величина РЕЕР обычно не оказывает отрицательного влияния на легочную механику и сердечно-сосудистую систему.
Потенциальные отрицательные эффекты высокого РЕЕР:
снижение венозного притока к сердцу;
повышение легочного сосудистого сопротивления;
перераспределение легочного кровотока в невентилируемые альвеолы;
Исследования, проведённые в 80-х годах прошлого века, показали, что повышение ЧД более 60 в мин приводит к лучшей синхронизации пациента с дыханием вентилятора, улучшает обмен газов в легких и снижает частоту баротравмы. При не медикаментозной синхронизации дыхания пациента и вентилятора, в острую фазу РДС, иногда используют ЧД 80-120 в мин (Твд 0.3 с). Однако необходимо помнить, что подобная стратегия может приводить к гипервентиляции с дыхательным алкалозом, отрицательными последствиями которой будут:
Снижение сердечного выброса.
Спазм мозговых сосудов.
Нарушение вентиляционно-перфузионных отношений.
В режиме А/С больной сам выбирает частоту принудительного дыхания, что является определённым преимуществом этого режима.
В настоящее время более важными считаются абсолютные величины Твд и Твыд, а не их соотношение. Минимальное Твд должно быть таково, чтобы пациент получил необходимый дыхательный объём, а короткое Твыд не должно приводить к появлению auto-PEEP. Учитывая короткую константу времени у больных РДС, вполне адекватным Твд будет 0.35 с, а у детей массой менее 1000 г менее 0.3 с. При превышении ЧД 60 в мин, для контроля за возможным развитием «auto-PEEP» желательно иметь графический монитор.
Особенности обеспечения синхронности дыхания пациента и аппарата ИВЛ.
У большинства новорождённых при проведении ИВЛ сохраняется спонтанное дыхание, но часто не синхронное с принудительными вдохами вентилятора. Сохранение самостоятельного дыхания чаще всего положительно влияет на обмен газов в легких и гемодинамику, но может и снижать эффективность ИВЛ. Это происходит, если новорождённый дышит:
1) с частотой дыхания отличной от установленной на вентиляторе и/или 2) с нерегулярным ритмом дыхания, а также в том случае если частота дыхания пациента и вентилятора одинаковы, но 3) не совпадают фазы вдоха и выдоха. Как правило, новорождённый форсированно дышит или «борется» с респиратором, если аппарат ИВЛ не обеспечивает ему адекватную минутную вентиляцию. Т.к. известно, что минутная вентиляция равна произведению дыхательного объёма на частоту, синхронизировать пациента с аппаратом ИВЛ можно, увеличив частоту респиратора или дыхательный объём (Piр), в случае если последний не превышает 6-7 млкг.
Существует два основных способа достижения синхронности дыхания пациента и вентилятора: перевод на принудительную ИВЛ (IMV) и пациент-триггерная вентиляция.
При IMV синхронизация достигается глубокой седатацией или миорелаксацией. Каждый из этих методов имеет свои специфические недостатки:
— Депрессия сердечно-сосудистой системы.
Увеличение продолжительности ИВЛ.
Увеличение продолжительности ИВЛ.
Спонтанное дыхание во время ИВЛ периодически снижает внутригрудное давление и способствует венозному притоку к сердцу, наполнению правого и левого желудочков, повышает сердечный выброс.
Принудительная вентиляция легких является оправданной только у пациентов:
с грубыми неврологическими нарушениями и т. н. «гипервентиляционным» синдромом, когда неконтролируемо высокая частота самостоятельных дыханий больного приводит к грубой гипервентиляции
с декомпенсированным метаболическим ацидозом
с сохраняющейся на пациент — триггерной вентиляции гипоксемией.
В остальных случаях предпочтительнее использовать пациент-триггерную вентиляцию.
Особые указания. При подборе параметров необходимо помнить, что:
1. Основными агрессивными параметрами ИВЛ, которые следует снижать в первую очередь, являются: PIP и FiO2 (> 40%).
2. За один раз давление меняется не более чем на 1-2смН2О, а частота не более чем на 5 вдохов. Лишь FiO2 может меняться под контролем SatO2 (88-92%) ступенчато на 5-10%.